题目内容
4.如图1是初中化学常用的实验装置,请根据实验要求选择适当的装置并完成相关问题.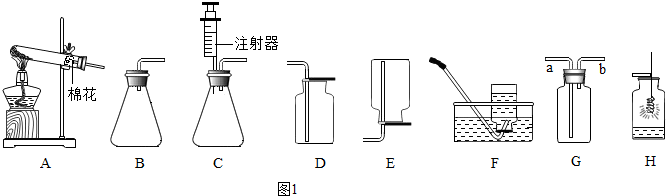
(1)分别用物质名称和化学符号写出实验室用氯酸钾制取氧气的化学反应表达式:氯酸钾 $→_{加热}^{二氧化锰}$氯化钾+氧气、2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,应选择的收集装置是D(或F、G)(填字母代号,下同),如果选用如装置G收集氧气,气体应从a(填“a”或“b”)端导入.
(2)某化学小组同学用20%的过氧化氢溶液和二氧化锰,并选用B装置来制取氧气,实验中,同学们发现不能得到平稳的氧气流,小明提出可将发生装置由B改为C,其理由是可控制液体的滴加速度,进而可控制反应速率.
(3)探究小组用装置H做“细铁丝在氧气中燃烧”的实验,但未看到“剧烈燃烧,火星四射”现象,你认为可能的原因是氧气的浓度低、铁丝表面的锈未除尽(合理均可)(答出一条即可),分别用物质名称和化学符号写出该反应的表达式:铁+氧气$\stackrel{点燃}{→}$四氧化三铁、3Fe+2O2 $\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(4)实验室常用加热无水醋酸钠与碱石灰固体混合物来制取甲烷气体.实验室制取甲烷应选用的发生装置是A.
(5)为探究“二氧化锰的质量对过氧化氢分解反应的影响”,小明又进行了如下实验,Ⅰ按如图甲组装实验仪器并进行密性检查;Ⅱ取10毫升溶质质量分数为3%的过氧化氢溶液和0.03克二氧化锰充分混合,用压强测量仪测量容器内的气压;Ⅲ倾斜装置,使过氧化氢溶液和二氧化锰充分混合,用压强测量仪测量容器内的气压;Ⅳ分别用0.06克、0.09克和0.12克相同的二氧化锰重复上述实验,整理相关数据如图丙.
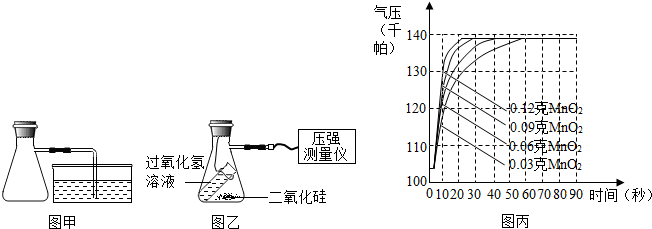
①写出步骤Ⅰ中检查装置气密性的具体操作及气密性良好的判断依据:用手捂住锥形瓶,导管口出现气泡,说明装置不漏气.
②实验中,小明用容器内压强的大小来反映产生氧气的多少.
③本实验除了研究“二氧化锰的质量对过氧化氢分解产生氧气质量的Ⅰ影响”外,还可以研究的问题是二氧化锰的质量对反应速率的影响.
④该探究过程得出的结论是过氧化氢分解产生氧气的质量与二氧化锰的质量无关(合理均可).
分析 (1)据反应原理书写表达式,氧气密度比空气大且不易溶于水,据此分析解答;
(2)注射器可控制液体的滴加速度,进而可控制反应速率,得到平稳的氧气流;
(3)据铁丝燃烧的注意事项和反应原理分析解答;
(4)加热无水醋酸钠与碱石灰固体混合物来制取甲烷气体属于固体加热型,故选发生装置A;
(5)①据检查气密性的方法分析解答;
②容器内压强越大,说明产生的氧气越多;
③根据图中数据还可以研究二氧化锰的质量对反应速率有无影响;
④据数据可以判断相关方面的问题.
解答 解:(1)氯酸钾在加热、二氧化锰作催化剂的条件下生成氯化钾和氧气,反应的文字或符号表达式分别是:氯酸钾 $→_{加热}^{二氧化锰}$氯化钾+氧气、2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(2)注射器可控制液体的滴加速度,进而可控制反应速率,得到平稳的氧气流;
(3)没有观察到“剧烈燃烧,火星四射”的现象的原因可能是:铁丝表面的锈未除尽;收集的氧气不纯;温度没有达到铁的着火点等;
铁与氧气反应生成四氧化三铁,反应的文字或符号表达式分别为:铁+氧气$\stackrel{点燃}{→}$四氧化三铁、3Fe+2O2 $\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(4)加热无水醋酸钠与碱石灰固体混合物来制取甲烷气体属于固体加热型,故选发生装置A;
(5)①步骤Ⅰ中检查装置气密性的具体操作及气密性良好的判断依据是:用手捂住锥形瓶,导管口出现气泡,则说明装置不漏气;
(2)实验中,容器内气体的压强越大,说明产生的氧气越多,压强越小,说明产生的氧气越少,因此小明是用容器内压强的大小来反映产生氧气的多少.
故填:容器内压强的大小.
(3)由图中数据可知,二氧化锰的质量大小能够影响反应的速率,但是不影响产生氧气的质量,因此本实验除了研究“二氧化锰质量对过氧化氢分解产生氧气质量的影响外”还可以研究的问题是二氧化锰的质量对反应速率的影响.
故答案为:(1)氯酸钾 $→_{加热}^{二氧化锰}$氯化钾+氧气、2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(2)可以控制液体的滴加速度;
(3)氧气的浓度低、铁丝表面的锈未除尽(合理均可);铁+氧气$\stackrel{点燃}{→}$四氧化三铁、3Fe+2O2 $\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(4)A;
(5)①用手捂住锥形瓶,导管口出现气泡,说明装置不漏气;
②容器内压强的大小;
③二氧化锰的质量对反应速率的影响;
④过氧化氢分解产生氧气的质量与二氧化锰的质量无关(或二氧化锰的质量越大,过氧化氢分解产生氧气的速率越快等).
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.故填:二氧化锰的质量对反应速率的影响.

 阅读快车系列答案
阅读快车系列答案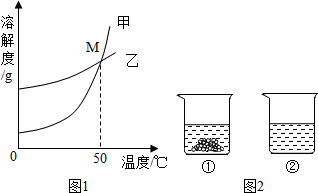 甲、乙固体的溶解度曲线如图1.40℃时,将等质量的甲、乙固体,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图2.下列说法正确的是( )
甲、乙固体的溶解度曲线如图1.40℃时,将等质量的甲、乙固体,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图2.下列说法正确的是( )| A. | ①中的固体是甲 | |
| B. | 将①中的溶液变为不饱和溶液,溶质质量分数一定减小 | |
| C. | ②中溶液一定不饱和 | |
| D. | ②中溶液降温至20℃时,溶质质量分数可能减小 |
 一些食品(如月饼)包装袋内常放有一小包干燥剂,如图是干燥剂袋上的部分文字,回答下列问题:
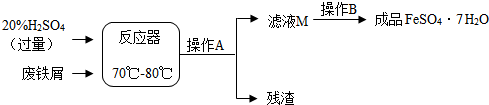
一些食品(如月饼)包装袋内常放有一小包干燥剂,如图是干燥剂袋上的部分文字,回答下列问题: 某碳酸钠样品含有少量的硫酸钠,取12g该样品完全溶解在水中配制成100g溶液,往其中滴入一定质量分数的稀硫酸至恰好完全反应,测定溶液的质量与加入稀硫酸的质量间的关系如图所示(生成的气体全部逸出).计算:
某碳酸钠样品含有少量的硫酸钠,取12g该样品完全溶解在水中配制成100g溶液,往其中滴入一定质量分数的稀硫酸至恰好完全反应,测定溶液的质量与加入稀硫酸的质量间的关系如图所示(生成的气体全部逸出).计算: 请根据燃烧条件的探究实验,回答问题:
请根据燃烧条件的探究实验,回答问题: