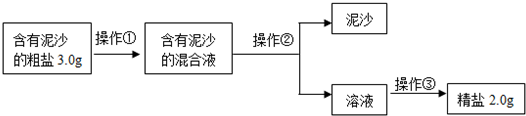
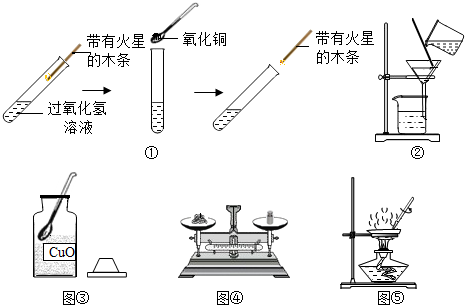
题目内容
5.某小组的同学在课外进行科学探究,以验证铜片在空气中灼烧后,表面生成的黑色物质确实是铜与氧气化合生成的CuO,他们进行了以下实验: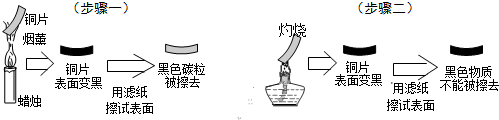
(1)由图两个实验步骤判断:铜片可能发生化学反应的是步骤二.(填“一”或“二”)
(2)为进一步证明步骤二铜片表面黑色物质的元素组成,他们选用了以下装置继续进行实验:
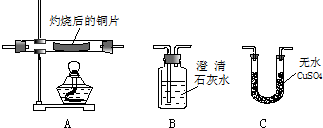
a.甲同学向A装置中通入纯净的H2,为检验反应产物,A的右边应连接上面的装置C
(填编号),所选装置的实验现象为白色无水硫酸铜变蓝,A装置中所发生的化学反应方程式为CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
b.乙同学向A装置中通入纯净的CO,A装置的实验现象为黑色的固体变成红色,为检验反应产物,A的右边应连接上面的装置B(填编号),所选装置中的实验现象为澄清石灰水变浑浊;此方法仅用上述装置有明显的缺陷,要弥补,应采取的措施是:加上一个尾气处理的装置.
c.通入的气体如果含有少量水蒸气,若在A装置左边增加一个B装置,则澄清石灰水应更换成浓硫酸.
d.对A装置加热前,应先通入纯净气体的目的是防止气体与空气混合加热发生爆炸.
(3)结论:经过甲、乙两同学的实验现象证明步骤二铜片表面的黑色物质为CuO.
分析 根据氧化铜的性质、氢气和一氧化碳还原氧化铜的现象、水和二氧化碳的检验方法进行分析解答,一氧化碳是有毒的气体,需要进行尾气处理,
解答 解:(1)烟熏的黑色碳粒能擦掉,说明发生的是物理变化,灼烧的黑色固体擦不掉,说明发生的是化学变化,故填:二;
(2)a.要检验氢气与氧化铜反应的产物,就是检验水的存在,可以加入无水硫酸铜,观察到无水硫酸铜变蓝,故填:C;白色无水硫酸铜变蓝;CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
b.一氧化碳能与氧化铜反应生成铜和二氧化碳,会观察到黑色的固体变为红色,要检验二氧化碳,可以使用澄清的石灰水,澄清的石灰水变浑浊,由于一氧化碳有毒,需要进行尾气处理,故填:黑色的固体变成红色;澄清石灰水变浑浊;加上一个尾气处理的装置;
c.要除去水,可以增加装有浓硫酸的装置,故填:浓硫酸;
d.对A装置加热前,应先通入纯净气体可以排出装置内的空气,防止气体与空气混合加热发生爆炸,故填:防止气体与空气混合加热发生爆炸;
(3)经过实验能证明步骤二铜片表面的黑色物质为CuO,故填:步骤二铜片表面的黑色物质为CuO.
点评 本题考查的是物质成分的实验探究,完成此题,可以依据已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.木炭和活性炭都具有很强的吸附能力,是由于( )
| A. | 都是无定形碳 | B. | 都是疏松多孔,表面积大 | ||
| C. | 它们的密度小 | D. | 其碳原子的排列方式不同 |
13.某化学兴趣小组取用2.0g石灰石样品,把25.0g质量分数为10%的稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如表:
请计算:
(1)2.0g石灰石样品中碳酸钙的质量为1.7g,石灰石中碳酸钙的质量分数为85%.
(2)请你继续计算反应生成溶液中溶质的质量分数(计算过程和结果均保留一位小数).
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 稀盐酸的累计加入量 | 5.0g | 10.0g | 15.0g | 20.0g | 25.0g |
| 剩余固体的质量 | 1.5g | 1.0g | 0.5g | 0.3g | 0.3g |
(1)2.0g石灰石样品中碳酸钙的质量为1.7g,石灰石中碳酸钙的质量分数为85%.
(2)请你继续计算反应生成溶液中溶质的质量分数(计算过程和结果均保留一位小数).
20.下列选项中,前者是化学变化,后者是物理性质的是( )
| A. | 食物腐败 钢铁生锈 | B. | 冰雪融化 牛奶变酸 | ||
| C. | 天然气燃烧 水结成冰 | D. | 烧杯炸裂 火药爆炸 |
15. 已知A、B、C、D、E 分别是铁、硝酸铜溶液、二氧化碳、稀硫酸溶液、氢氧化钠溶液中的一种,A 是硝酸铜溶液.有关物质之间转换关系如图所示,其中“-”表示物质之间能发生化学反应.下列说法正确的是( )
已知A、B、C、D、E 分别是铁、硝酸铜溶液、二氧化碳、稀硫酸溶液、氢氧化钠溶液中的一种,A 是硝酸铜溶液.有关物质之间转换关系如图所示,其中“-”表示物质之间能发生化学反应.下列说法正确的是( )
 已知A、B、C、D、E 分别是铁、硝酸铜溶液、二氧化碳、稀硫酸溶液、氢氧化钠溶液中的一种,A 是硝酸铜溶液.有关物质之间转换关系如图所示,其中“-”表示物质之间能发生化学反应.下列说法正确的是( )
已知A、B、C、D、E 分别是铁、硝酸铜溶液、二氧化碳、稀硫酸溶液、氢氧化钠溶液中的一种,A 是硝酸铜溶液.有关物质之间转换关系如图所示,其中“-”表示物质之间能发生化学反应.下列说法正确的是( )| A. | B是氢氧化钠溶液 | |
| B. | 反应①和反应③属于同一种反应类型 | |
| C. | 反应②产生的实验现象是有气泡产生,溶液逐渐变为黄色 | |
| D. | 实验室制取E的反应原理是:2HCl+CaCO3═CaCl2+H2O+CO2↑ |