题目内容
13.某化学兴趣小组取用2.0g石灰石样品,把25.0g质量分数为10%的稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如表:| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 稀盐酸的累计加入量 | 5.0g | 10.0g | 15.0g | 20.0g | 25.0g |
| 剩余固体的质量 | 1.5g | 1.0g | 0.5g | 0.3g | 0.3g |
(1)2.0g石灰石样品中碳酸钙的质量为1.7g,石灰石中碳酸钙的质量分数为85%.
(2)请你继续计算反应生成溶液中溶质的质量分数(计算过程和结果均保留一位小数).
分析 (1)固体剩余的质量是杂质的质量,由杂质的质量可计算出石灰石中碳酸钙的质量,由碳酸钙的质量可计算出石灰石中碳酸钙的质量分数;
(2)由碳酸钙的质量可以根据化学方程式计算出生成氯化钙的质量和二氧化碳的质量,进而计算出生成溶液中氯化钙的质量分数.
解答 解:(1)最后剩余的0.3克为杂质质量,所以石灰石中碳酸钙的质量为2g-0.3g=1.7g;
石灰石中碳酸钙的质量分数为$\frac{1.7g}{2g}$×100%=85%.
(2)设生成CaCl2的质量为x,生成CO2的质量为y.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
1.7g x y
$\frac{100}{1.7g}=\frac{111}{x}=\frac{44}{y}$
x≈1.9g,y≈0.7g
生成溶液中氯化钙的质量分数为$\frac{1.9g}{1.7g+25g-0.7g}$×100%≈7.3%
答:(1)2.0g石灰石样品中碳酸钙的质量为1.7g,石灰石样品中碳酸钙的质量分数为85%;
(2)反应生成溶液中氯化钙的质量分数为7.3%.
点评 本题考查有关化学方程式的计算和溶质质量分数的计算,难度较大.

练习册系列答案
相关题目
3.下面是某化学反应的微观模型示意图,据此分析错误的是( )
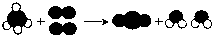

| A. | 反应前后原子数目没有变化 | B. | 反应的本质是原子的重新组合过程 | ||
| C. | 分子是由原子构成的 | D. | 反应前后分子不变 |
1. 水和溶液在生命活动和生产、生活中起着十分重要的作用.
水和溶液在生命活动和生产、生活中起着十分重要的作用.
(1)“生命吸管”(如图)是一种可以随身携带的小型水净化器,里面装有网丝、注入了活性炭和碘的树脂等.其中活性炭起到吸附和过滤作用.
(2)水常用来配制各种溶液,硫酸铜溶液中的溶质为CuSO4.(填化学式)
(3)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种.这是利用物质的物理性质.(填“物理”或“化学”)
(4)根据表回答问题.
①60℃时,向两个分别盛有38g NaCl和NH4Cl的烧杯中,各加入100g水,充分溶解后,NaCl溶液为饱和溶液.
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液.下列说法正确的是D(填字母序号)
A.溶质的质量不变 B.溶液中溶质的质量分数一定减小
C.溶液质量可能不变 D.可升高温度或增加溶剂.
 水和溶液在生命活动和生产、生活中起着十分重要的作用.
水和溶液在生命活动和生产、生活中起着十分重要的作用.(1)“生命吸管”(如图)是一种可以随身携带的小型水净化器,里面装有网丝、注入了活性炭和碘的树脂等.其中活性炭起到吸附和过滤作用.
(2)水常用来配制各种溶液,硫酸铜溶液中的溶质为CuSO4.(填化学式)
(3)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种.这是利用物质的物理性质.(填“物理”或“化学”)
(4)根据表回答问题.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.5 | 37.3 | 38.4 | 39.8 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液.下列说法正确的是D(填字母序号)
A.溶质的质量不变 B.溶液中溶质的质量分数一定减小
C.溶液质量可能不变 D.可升高温度或增加溶剂.
18.在一定温度下,把ag物质加入bg水中,则所得溶液的质量( )
| A. | 小于(a+b)g | B. | 等于(a+b)g | C. | 大于(a+b)g | D. | 不大于(a+b)g |
3.2016年1月6日襄阳市首次启动空气严重污染黄色预警.下列各项与形成雾霾无关的是( )
| A. | 工业粉尘 | B. | 汽车尾气 | C. | 煤炭燃烧 | D. | 风力发电 |
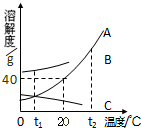 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答: