题目内容
1.归纳推理是学习化学的重要方法之一.下列有关事实的推理、结论合理的是( )| A. | 酸与碱反应生成盐和水.生成盐和水的反应一定是酸与碱的反应 | |
| B. | 有机化合物是含碳元素的化合物.甲烷和酒精均属于有机化合物 | |
| C. | 金刚石和石墨均是由碳元素组成的单质.金刚石和石墨是同一种物质 | |
| D. | 碱溶液的pH大于7.碳酸氢钠溶液的pH大于7,所以碳酸氢钠属于碱 |
分析 A、中和反应是酸与碱作用生成盐和水的反应,反应物是酸和碱,生成物是盐和水,进行分析判断.
B、含有碳元素的化合物叫有机化合物,简称有机物.
C、根据常见的碳单质,进行分析判断.
D、根据当溶液的pH大于7时,呈碱性,结合碳酸氢钠的分类,进行分析判断.
解答 解:A、酸与碱反应生成盐和水,但生成盐和水的反应不一定是酸与碱的反应,如CO2+2NaOH═Na2CO3+H2O,故选项推理错误.
B、有机化合物是含碳元素的化合物,甲烷和酒精均是含碳元素的化合物,均属于有机化合物,故选项推理正确.
C、金刚石和石墨均是由碳元素组成的单质,金刚石和石墨不是同一种物质,是碳元素形成的不同单质,故选项推理错误.
D、碱溶液的pH大于7.碳酸氢钠溶液的pH大于7,但碳酸氢钠是由钠离子和碳酸氢根离子构成的化合物,属于盐,故选项推理错误.
故选:B.
点评 本题难度不大,掌握中和反应的特征、有机物的特征、碳元素形成的单质、盐的特征等并能灵活运用是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1. 往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续加入质量为m的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法中正确的是( )
往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续加入质量为m的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法中正确的是( )
 往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续加入质量为m的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法中正确的是( )
往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续加入质量为m的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法中正确的是( )| A. | c点对应溶液中含有的金属离子为Zn2+和Cu2+ | |
| B. | bc段(不含两端点)析出的金属是Fe | |
| C. | ab段(不含两端点)对应溶液中含有的金属离子为Zn2+、Ag+、Cu2+和Fe2+ | |
| D. | 若bc段和cd段中析出固体质量相等,参加反应的锌粉质量分别为m1和m2,则m1>m2 |
12.将适量的碳酸钙粉末加入到盛有83.2克稀盐酸的烧杯中,立即将烧杯放在天平上称量.在以后的8min内,每一分钟读一次数(最后二者恰好完全反应).结果如下
请分析并解答下列问题(前3小题直接把答案写在横线处,第4小题写出解题过程):
(1)烧杯中物质质量减少的原因是反应生成的二氧化碳逸出
(2)在该反应中,会发现随着反应的进行,反应速度越来越小,这说明反应速度与反应物的浓度有关
(3)有表格可看出,反应完全结束的时间是在第6分钟
(4)计算反应后溶液的溶质质量分数.
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 质量/g | 93.2 | 91.4 | 90.2 | 89.5 | 89.1 | 88.9 | 88.8 | 88.8 | 88.8 |
(1)烧杯中物质质量减少的原因是反应生成的二氧化碳逸出
(2)在该反应中,会发现随着反应的进行,反应速度越来越小,这说明反应速度与反应物的浓度有关
(3)有表格可看出,反应完全结束的时间是在第6分钟
(4)计算反应后溶液的溶质质量分数.
6.下列实验操作正确或实验设计能达到实验目的是( )
| A. |  添加酒精 | B. |  探究燃烧条件 | C. |  蒸发操作 | D. |  过滤操作 |
10.课本上有8个“基础实验”,以提升同学们的实验能力,以下叙述正确的是( )
| A. | “粗盐的初步提纯”实验中,持续加热食盐溶液直至水分蒸干 | |
| B. | “溶液的酸碱性”实验中,将pH试纸伸入溶液中测定酸碱度 | |
| C. | “氧气的制取与性质”实验中,做铁丝燃烧实验的集气瓶内要预留少量的水 | |
| D. | “酸与碱的化学性质”实验中,将实验废液直接倒入下水道 |
11.下列四个图象中有关量的变动趋势与对应的叙述关系正确的是( )


| A. | 将等质量的锌粉和铁粉,分别放入两份溶质质量分数相同且足量的稀盐酸中 | |
| B. | 一定质量的红磷在密闭容器中燃烧 | |
| C. | 向氢氧化钠溶液中不断加水稀释 | |
| D. | 加热一定质量的氯酸钾和二氧化锰混合物至完全分解 |
 如图为金属相框构造图
如图为金属相框构造图 ”表示Fe2+.(填写微粒的符号)
”表示Fe2+.(填写微粒的符号)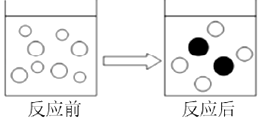
 固体氢氧化钠放置在空气中容易变质转化为碳酸钠.现称取一久置于空气中的烧碱样品12.6g完全溶于蒸馏水中配成100g溶液,向其中滴加质量分数为8.55%的氢氧化钡溶液,产生沉淀与所加氢氧化钡溶液的质量关系如图所示.请通过计算回答:
固体氢氧化钠放置在空气中容易变质转化为碳酸钠.现称取一久置于空气中的烧碱样品12.6g完全溶于蒸馏水中配成100g溶液,向其中滴加质量分数为8.55%的氢氧化钡溶液,产生沉淀与所加氢氧化钡溶液的质量关系如图所示.请通过计算回答: