题目内容
13. 固体氢氧化钠放置在空气中容易变质转化为碳酸钠.现称取一久置于空气中的烧碱样品12.6g完全溶于蒸馏水中配成100g溶液,向其中滴加质量分数为8.55%的氢氧化钡溶液,产生沉淀与所加氢氧化钡溶液的质量关系如图所示.请通过计算回答:
固体氢氧化钠放置在空气中容易变质转化为碳酸钠.现称取一久置于空气中的烧碱样品12.6g完全溶于蒸馏水中配成100g溶液,向其中滴加质量分数为8.55%的氢氧化钡溶液,产生沉淀与所加氢氧化钡溶液的质量关系如图所示.请通过计算回答:(1)a的值200.
(2)当沉淀刚好达到最大质量时,溶液中溶质质量为多少g?
分析 (1)根据化学方程式和生成沉淀的质量计算参加反应的氢氧化钡的质量;
(2)根据质量守恒定律计算反应后溶液的质量,依据化学方程式计算生成溶质的质量,然后计算反应后,溶液中溶质的质量分数.
解答 解:设参加反应的碳酸钠的质量为x,参加反应的氢氧化钡的质量为y,生成氢氧化钠的质量为z
Ba(OH)2+Na2CO3=BaCO3↓+2NaOH
171 106 197 80
y x 19.7g z
$\frac{171}{y}=\frac{106}{x}=\frac{197}{19.7g}=\frac{80}{z}$
x=10.6g
y=17.1g
z=8g
(1)a=$\frac{17.1g}{8.55%}$=200g;
(2)溶液中溶质NaOH的质量分数为$\frac{8g+(12.6g-10.6g)}{100g+200g-19.7g}$×100%=3.57%.
故答案为:(1)200;
(2)溶液中溶质NaOH的质量分数为3.57%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.如图是某化学反应的微观示意图,其中“ ”和“
”和“ ”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质,下列关于该反应前、后的说法不正确的是( )
”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质,下列关于该反应前、后的说法不正确的是( )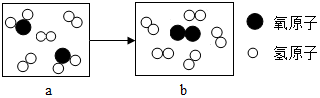
 ”和“
”和“ ”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质,下列关于该反应前、后的说法不正确的是( )
”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质,下列关于该反应前、后的说法不正确的是( )
| A. | 反应前后原子总数不变 | B. | a、b均为混合物 | ||
| C. | 该反应为分解反应 | D. | a中两种物质均为化合物 |
1.归纳推理是学习化学的重要方法之一.下列有关事实的推理、结论合理的是( )
| A. | 酸与碱反应生成盐和水.生成盐和水的反应一定是酸与碱的反应 | |
| B. | 有机化合物是含碳元素的化合物.甲烷和酒精均属于有机化合物 | |
| C. | 金刚石和石墨均是由碳元素组成的单质.金刚石和石墨是同一种物质 | |
| D. | 碱溶液的pH大于7.碳酸氢钠溶液的pH大于7,所以碳酸氢钠属于碱 |
8.液氨可用作清洁燃料,其燃烧时的主要反应为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2X+6H2O.下列有关说法中不正确的是( )
| A. | X的化学式为N2 | B. | 上述反应的类型属于置换反应 | ||
| C. | 液氨属于化合物 | D. | 反应前后氨元素的化合价降低 |
18.山东大学教授团队通过简单的纺丝手段设计制备了三氧化钨“可复写纤维薄膜”.三氧化钨(WO3)本身没有颜色,但在电场或者紫外线光的作用下能够被还原为有颜色的还原态,再经过氧化反应又可以回到无色状态,这种在外界刺激下能够发生可逆颜色变化的特性使三氧化钨备受关注.下列说法正确的是( )
| A. | 三氧化钨是氧化物 | |
| B. | 三氧化钨中钨元素和氧元素的质量比是1:3 | |
| C. | 三氧化钨中钨元素显+3价 | |
| D. | 三氧化钨在通常情况下可以自动变色 |
2.下列气体不会产生温室效应的是( )
| A. | 甲烷 | B. | 二氧化碳 | C. | 一氧化碳 | D. | 臭氧 |
3. 联合国确定2017年“世界水日”的宣传主题是“Wastewater”(废水),我国纪念2017年“世界水日”和“中国水周”活动的宣传主题为“落实绿色发展理念,全面推行河长制”.巢湖是五大淡水湖之一,为了防止巢湖水受到污染,合肥投千亿治理修复环巢湖生态,改善巢湖水质.下列做法容易造成巢湖水体污染的是:( )
联合国确定2017年“世界水日”的宣传主题是“Wastewater”(废水),我国纪念2017年“世界水日”和“中国水周”活动的宣传主题为“落实绿色发展理念,全面推行河长制”.巢湖是五大淡水湖之一,为了防止巢湖水受到污染,合肥投千亿治理修复环巢湖生态,改善巢湖水质.下列做法容易造成巢湖水体污染的是:( )
 联合国确定2017年“世界水日”的宣传主题是“Wastewater”(废水),我国纪念2017年“世界水日”和“中国水周”活动的宣传主题为“落实绿色发展理念,全面推行河长制”.巢湖是五大淡水湖之一,为了防止巢湖水受到污染,合肥投千亿治理修复环巢湖生态,改善巢湖水质.下列做法容易造成巢湖水体污染的是:( )
联合国确定2017年“世界水日”的宣传主题是“Wastewater”(废水),我国纪念2017年“世界水日”和“中国水周”活动的宣传主题为“落实绿色发展理念,全面推行河长制”.巢湖是五大淡水湖之一,为了防止巢湖水受到污染,合肥投千亿治理修复环巢湖生态,改善巢湖水质.下列做法容易造成巢湖水体污染的是:( )| A. | 严格控制在巢湖内的网箱养殖水产 | |
| B. | 在农业生产过程中提倡施用农家肥 | |
| C. | 沿巢湖工厂的工业废水经处理后排入巢湖 | |
| D. | 沿巢湖周边居民生活废水直接排入巢湖 |