题目内容
15.炼铁的主要原料是铁矿石,用赤铁矿(主要成分为Fe2O3)炼铁的反应原理为3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(1)Fe2O3中铁元素的质量分数为:70%
(3)用含Fe2O360%的赤铁矿石800t,理论上可炼出纯铁多少吨?(写出计算过程及结果)
分析 (1)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(2)由赤铁矿石的质量、氧化铁的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出理论上可炼出铁的质量.
解答 解:(1)Fe2O3的相对分子质量为56×2+16×3=160,Fe2O3中铁元素的质量分数为$\frac{56×2}{160}$100%=70%.
(2)设理论上可炼出铁的质量为x.
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
800t×60% x
$\frac{160}{800t×60%}=\frac{112}{x}$
x=336t
答:
(1)Fe2O3中铁元素的质量分数为70%;
(2)理论上可炼出铁的质量为336t.
点评 本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.

练习册系列答案
相关题目

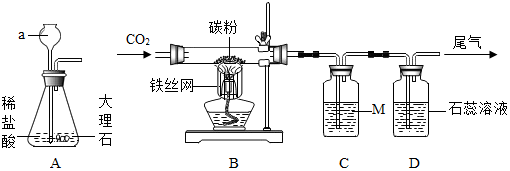
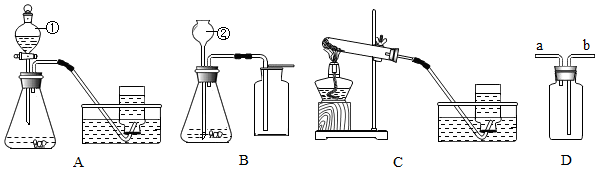
 某化学兴趣小组为了测定某石灰石样品的纯度,小组同学取出12.5g石灰石样品粉碎后盛放于烧杯中(样品中杂质不溶于水,且不与酸反应),然后往烧杯中逐渐加入稀盐酸,充分反应后产生气体的质量与反应时间的关系如图,请计算:
某化学兴趣小组为了测定某石灰石样品的纯度,小组同学取出12.5g石灰石样品粉碎后盛放于烧杯中(样品中杂质不溶于水,且不与酸反应),然后往烧杯中逐渐加入稀盐酸,充分反应后产生气体的质量与反应时间的关系如图,请计算: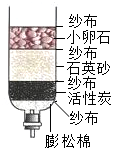 水资源的保护和合理利用已受到人们的普遍关注.请你参与讨论下列问题:
水资源的保护和合理利用已受到人们的普遍关注.请你参与讨论下列问题: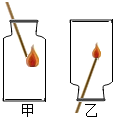 装满氧气的甲、乙两个集气瓶(甲瓶口向上,乙瓶口向下),用带火星的木条分别由瓶口伸入瓶底,发现木条复燃且甲燃烧比乙旺.上述实验说明了氧气具有的性质是:
装满氧气的甲、乙两个集气瓶(甲瓶口向上,乙瓶口向下),用带火星的木条分别由瓶口伸入瓶底,发现木条复燃且甲燃烧比乙旺.上述实验说明了氧气具有的性质是: