题目内容
6.某化学兴趣小组对金属的性质做了如下探究,请你填写空格:
(1)用如图所示实验探究铁生锈的条件(每支试管中均放有完全相同的洁净铁钉)
①甲同学认为,试管A发生的现象就能够说明铁的锈蚀是铁与空气中的氧气、水蒸气共同作用的结果.乙同学不同意他的观点,认为必须全面观察试管ABC(填试管编号)发生的现象,并经过科学严谨的推理,才能得出上述结论.
②试管D和E实验的目的是进一步探究铁在盐、酸存在的环境中是否更容易锈蚀.
③为防止金属锈蚀,除了采用覆盖保护膜等措施以外,还可以制成合金.这是因为合金与纯金属相比,其组成和内部组织结构发生变化,从而引起性质的变化.
(2)某同学向分别盛有等质量的铁粉和锌粒的试管中,倒入等质量、等溶质质量分数的稀硫酸,以“金属表面产生气泡的快慢”为标准来判断两种金属的活动性强弱.有的同学认为这种方案不够合理,理由是等质量的铁粉和锌粒与稀硫酸的接触面积不同
(3)将一定质量的铁粉放入硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,所得固体中一定含有的物质是铜,且反应后溶液中一定存在的溶质是硝酸锌、硝酸亚铁,质量比反应前减小(填“增大”“减小”或“不变”).
分析 铁和水、氧气同时接触时容易生锈,盐溶液、酸溶液能够促进铁生锈;
物质的结构不同,性质就不同;
进行对比试验要确定好常量和变量;
锌比铁活泼,铁比铜活泼.
解答 解:(1)①通过B可知,在没有氧气的情况下铁不容易生锈,通过C可知,在没有水的情况下铁不容易生锈,A中的铁和水、氧气同时接触容易生锈,通过ABC可知,铁在水和氧气同时存在的情况下容易生锈.
故填:ABC.
②试管D和E中,铁钉 与水和氧气接触的同时和盐、酸接触,目的是进一步探究铁在盐、酸存在的环境中是否更容易锈蚀.
故填:盐、酸存在.
③合金与纯金属相比,其组成和内部组织结构发生变化,从而引起性质的变化.
故填:性质.
(2)这种方案不够合理的理由是等质量的铁粉和锌粒与稀硫酸的接触面积不同,无法比较铁和锌的活泼性.
故填:等质量的铁粉和锌粒与稀硫酸的接触面积不同.
(3)将一定质量的铁粉放入硝酸铜、硝酸锌的混合溶液中,铁不如锌活泼,因此铁不能和硝酸锌反应,铁比铜活泼,因此铁能和硝酸铜反应生成硝酸亚铁和铜,充分反应后过滤,所得固体中一定含有的物质是铜,反应后溶液中一定存在的溶质是没有反应的硝酸锌和反应生成的硝酸亚铁;
铁和硝酸铜反应的化学方程式及其反应物、生成物的质量关系为:Fe+CuSO4═FeSO4+Cu,
56 64
由反应物、生成物质量关系可知,每56份质量的铁反应生成64份质量的铜,随着反应的进行,溶质质量在减小.
故填:铜;硝酸锌、硝酸亚铁;减小.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案 有形状相同的A、B两种金属放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论不合理的是( )
有形状相同的A、B两种金属放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论不合理的是( )| A. | 金属的活动性B>A | B. | 生成氢气的质量A>B | ||
| C. | 反应的硫酸质量A>B | D. | 反应的金属质量A>B |
| A. | 氧化镁(MgO) | B. | 氧化钠 (NaO) | C. | 硫酸锌(ZnSO4 ) | D. | 氢氧化铜﹙Cu(OH)2﹚ |
| A. | 氧气分子变小 | B. | 氧气分子间间隔变小 | ||
| C. | 氧气分子在不断运动 | D. | 氧气分子变成了臭氧分子(O3) |
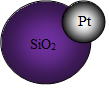 纳米球异质二聚体是纳米自动化产业中的一种新模型.不溶于水的二氧化硅晶体可以制成微小的纳米球.在铂的催化作用下,双氧水分解,同时使一个二氧化硅纳米球与一个铂纳米球相结合,构成了一个纳米球异质二聚体(如图所示),这就是一个纳米级发动机.它可望用于河流和溪水的污染控制以及人体内部器官和细胞的运行.根据以上信息判断,下列有关说法错误的是( )
纳米球异质二聚体是纳米自动化产业中的一种新模型.不溶于水的二氧化硅晶体可以制成微小的纳米球.在铂的催化作用下,双氧水分解,同时使一个二氧化硅纳米球与一个铂纳米球相结合,构成了一个纳米球异质二聚体(如图所示),这就是一个纳米级发动机.它可望用于河流和溪水的污染控制以及人体内部器官和细胞的运行.根据以上信息判断,下列有关说法错误的是( )| A. | 二氧化硅纳米球中含有的硅、氧原子个数比为1:2 | |
| B. | 纳米球异质二聚体,其微粒大小在纳米级范围 | |
| C. | 双氧水分解时,二氧化硅不是催化剂 | |
| D. | 因为二氧化硅晶体能与水反应而溶解,所以该纳米级发动机可以用于水污染的控制 |