题目内容
16.某课外活动小组在学习了书本“空气中氧气含量的测定”实验后,知道了五氧化二磷不能随便排放在空气中,否则会对空气造成污染,所以对该实验进行了改进:
在由两个注射器组成的密闭系统内共有50mL空气,如图1.然后给装有红磷的玻璃管加热.同时推动两个注射器的活塞,至玻璃管内的红磷变成白烟,且较长时间内无进一步变化时停止.停止加热后,待冷却至室温将气体全部推至一个注射器内.请根据你对上述实验的理解,回答下列问题:
(1)图1实验中观察到的现象是红磷燃烧,产生了大量的白烟,放热.红磷足量的目的是耗尽集气瓶中的氧气
若用图I装置实验结果是:空气中氧气含量小于空气总体积$\frac{1}{5}$,其操作上的原因可能是装置气密性不好.空气中氧气含量大于空气总体积$\frac{1}{5}$弹簧夹没夹紧.(各写出一点即可)
(2)图2实验结束后,注射器内的气体体积理论上应该减少约10mL.在实验的加热过程中,交替缓慢推动两个注射器的目的是使空气中的氧气与铜充分反应. 写出该反应的文字表达式氧气+铜$\stackrel{加热}{→}$氧化铜.
(3)某同学由本实验得到如下一些结论:①燃烧匙中红磷越多,水位上升越高.②空气中含有氮气、氧气、二氧化碳和稀有气体.③可用木炭替红磷完成该实验.④氮气难溶于水.其中正确的是:④(填序号).
分析 (1)运用燃烧法测定空气中氧气的体积分数,需将氧气全部消耗掉该实验中红磷需稍过量,目的是为了耗尽集气瓶中的氧气;
(2)根据空气的组成可以知道,氧气约占空气体积的五分之一,所以小红实验过程中出现的现象是密闭容器内气体的体积约减少5mL,可以据此解答.
该反应中铜与氧气在加热条件下反应生成氧化铜,可以据此解答.小红在实验的加热过程中,交替缓慢推动两注射器的目的是使空气中的氧气与铜充分反应可以据此解答.
(3)根据测定时可以使用红磷燃烧消耗氧气使瓶内压强减小的方法,磷燃烧能生成五氧化二磷;进行此实验时,必须保证装置的气密性良好,红磷足量,瓶子冷却后再打开弹簧夹,否则会导致结果不准确,不能用木炭、硫等燃烧后生成气体的物质来替代红磷.
解答 解:(1)图1实验中观察到的现象是:红磷燃烧,产生了大量的白烟,放热;测定空气中氧气的体积分数,需将氧气全部消耗掉该实验中红磷需稍过量,目的是为了耗尽集气瓶中的氧气;若用图I装置实验结果是:空气中氧气含量小于空气总体积$\frac{1}{5}$,其操作上的原因可能是:装置气密性不好;红磷不足;没有冷却至室温就打开止水夹;空气中氧气含量大于空气总体积$\frac{1}{5}$,可能是弹簧夹没夹紧;
(2)根据空气的组成可以知道,氧气约占空气体积的五分之一,所以实验过程中出现的现象是密闭容器内气体的体积约减少10mL.在实验的加热过程中,交替缓慢推动两注射器的目的是使空气中的氧气与铜充分反应.该反应中铜与氧气在加热条件下反应生成氧化铜,该反应的文字表达式为:氧气+铜$\stackrel{加热}{→}$氧化铜.
(3)如下这些结论中:①燃烧匙中的红磷越多,水位上升越高;错误,因为空气中氧气的体积是一定的;②空气含有氮气、氧气、二氧化碳和稀有气体;错误,此实验不能证明空气中有氮气、二氧化碳和稀有气体;③可用木炭代替红磷完成该实验;错误,木炭燃烧生成二氧化碳,瓶内气压变化较小;④氮气难溶于水;结论正确,故选④.
答案为:
(1)红磷燃烧,产生了大量的白烟,放热;耗尽集气瓶中的氧气;装置气密性不好;弹簧夹没夹紧;
(2)10;使空气中的氧气与铜充分反应;氧气+铜$\stackrel{加热}{→}$氧化铜;
(3)④.
点评 本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,难度不大,能够考查学生分析问题能力.

 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案| 反应时间min | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 反应后固体的质量g | 60 | 56.8 | 53.6 | 50.4 | 47.2 | 44 | 44 | 44 |
(2)在氯酸钾中,钾元素与氧元素的质量比为13:16;
(3)求原混合固体中氯酸钾的质量,并写出计算过程;
(4)求60克氯酸钾和二氧化锰的混合物中二氧化锰的质量分数,并写出计算过程.
 空气中氧气含量测定的再认识.
空气中氧气含量测定的再认识.【实验回顾】如图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
(1)写出红磷燃烧的化学方程式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内压强减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值较大.
【实验改进】
Ⅰ.根据铁在空气中生锈的原理设计如图2实验装置,再次测定空气中氧气的含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表:
| 测量项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
| 体积/mL | 80.0 | 54.5 | 126.0 |
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式2Fe+O2+2H2O=2Fe(OH)2.
(2)根据表中数据,改进实验后测得的空气中氧气的体积分数是20.2%(计算结果精确到0.1%).
(3)从实验原理角度分析,改进后的实验结果比前者准确度更髙的原因是:
①氧气完全反应;
②避免了燃烧匙伸入集气瓶中时导致的空气外逸.
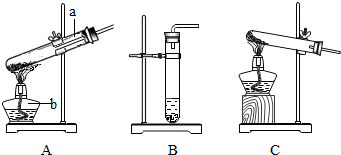

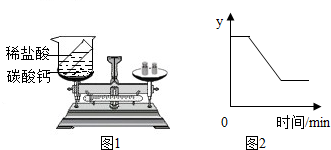 根据质量守恒定律,回答下列问题.Ⅰ、为验证质量守恒定律,某同学设计了如图的实验.
根据质量守恒定律,回答下列问题.Ⅰ、为验证质量守恒定律,某同学设计了如图的实验.