��Ŀ����
7��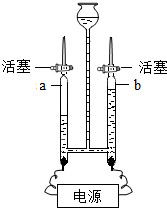 ����ͼװ�ý���ˮ�ĵ��ʵ�飮
����ͼװ�ý���ˮ�ĵ��ʵ�飮��1����ʼ��Ӧǰa��b�����ڲ�����Һ�壬�رջ�������ͨ��Դ��һ��ʱ������ܲ�����������ͼ��ʾ����a���·�����Ӧ�ӵ�Դ�ĸ�������������������ô����ǵ�ľ����֤b���е����壬д�����ˮ�Ļ�ѧ����ʽ��2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2H2��+O2����
��2��˵��ˮ��һ�ֻ������ʵ��~ʵ��ˮ�ֽ�������������������
���� ���ݵ��ˮ��֪ʶ���з�����ɣ�
��� �⣺
��1��a�ܲ���������϶࣬��������˵�����Դ�ĸ���������b�ܲ����������������ô����ǵ�ľ�����飬���ˮʱ���ɵ���������������������������ǵ�ľ����2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2H2��+O2����
��2�����ˮʱ������������������˵��ˮ�к�����Ԫ�غ���Ԫ�أ��Ӷ�˵��ˮ�ǻ�������ˮ�ֽ�������������������
�𰸣�
��1�����������ǵ�ľ����2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2H2��+O2����
��2��ˮ�ֽ�������������������
���� ���⿼����ˮ���й�֪ʶ����ɴ��⣬�����������е�֪ʶ���У�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
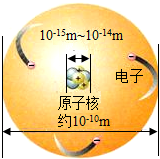
2��ԭ�ӵĽṹʾ��ͼ��ͼ������������ȷ���ǣ�������

| A�� | ԭ�ӡ����ӡ����Ӿ��ȵķ�ɢ��ԭ���� | |
| B�� | ���Ӵ����磬���Ӵ����磬����ԭ�Ӳ��Ե��� | |
| C�� | ͬһԭ���У����������������� | |
| D�� | ���������������� |
12��ij��ȤС���ͬѧΪ��֤�����Ļ�ѧ���ʣ���ʵ�����ォһС���ͭ��ͭп�Ͻ𣩷����ձ��У�����һ������ϡ���ᣬ��ַ�Ӧ����˵ù������Һ������˵������ȷ���ǣ�������
| A�� | ��Ӧ����Һ������һ�����ڷ�Ӧǰ��Һ���� | |
| B�� | ��Һ�е�����һ����������п | |
| C�� | ��Һ�е�����һ������������ | |
| D�� | ��Ӧ��ʣ��Ĺ�����һ������ͭ |
19�� �����ǵ���Ҫ�ɷ���̼��ƣ�Ϊ�ⶨ�������е�̼��ƺ�����ijͬѧ��������ϴ������ָ��ﲢ���飬չ��������̽����
�����ǵ���Ҫ�ɷ���̼��ƣ�Ϊ�ⶨ�������е�̼��ƺ�����ijͬѧ��������ϴ������ָ��ﲢ���飬չ��������̽����
��1����������������Ϊ35%��Ũ�������Ƴ�10%��ϡ���ᣬ��������Ϊ��
����1����������Ũ�����ˮ�������
����2�����ݼ�����������Ͳ�����������ƣ��ֱ���ȡ�����Ũ�����ˮ��
����3����Ũ���ᵹ��ˮ�в��ò���������õ�ϡ���ᣮ
��2����ø��Ե�������������������ͼ��ʾ����ƿ�У���Һ©���еĻ�����ʹ���ַ�Ӧ��ֱ�����ٲ�������Ϊֹ������װ���е�ϡ�����������������е��������ʲ���ϡ���ᷴӦ����ʵ�����ݼ�¼���±���
��CaCO3+2HCl=CaCl2+H2O+CO2����
�����ü�������̼��Ƶ�����������
 �����ǵ���Ҫ�ɷ���̼��ƣ�Ϊ�ⶨ�������е�̼��ƺ�����ijͬѧ��������ϴ������ָ��ﲢ���飬չ��������̽����
�����ǵ���Ҫ�ɷ���̼��ƣ�Ϊ�ⶨ�������е�̼��ƺ�����ijͬѧ��������ϴ������ָ��ﲢ���飬չ��������̽������1����������������Ϊ35%��Ũ�������Ƴ�10%��ϡ���ᣬ��������Ϊ��
����1����������Ũ�����ˮ�������
����2�����ݼ�����������Ͳ�����������ƣ��ֱ���ȡ�����Ũ�����ˮ��
����3����Ũ���ᵹ��ˮ�в��ò���������õ�ϡ���ᣮ
��2����ø��Ե�������������������ͼ��ʾ����ƿ�У���Һ©���еĻ�����ʹ���ַ�Ӧ��ֱ�����ٲ�������Ϊֹ������װ���е�ϡ�����������������е��������ʲ���ϡ���ᷴӦ����ʵ�����ݼ�¼���±���
��CaCO3+2HCl=CaCl2+H2O+CO2����
| ��Ӧǰ | �����ǵ����� | 16�� |
| װ�ú�ϡ����������� | 220�� | |
| ��Ӧ�� | װ�ü���������������� | 231.6�� |
18�����������У����������ӹ��ɵ��ǣ�������
| A�� | ������̼ | B�� | �Ȼ�þ | C�� | ���� | D�� | ˮ |





