题目内容
19. 鸡蛋壳的主要成分是碳酸钙,为测定鸡蛋壳中的碳酸钙含量,某同学将鸡蛋壳洗净、充分干燥并捣碎,展开了下列探究:
鸡蛋壳的主要成分是碳酸钙,为测定鸡蛋壳中的碳酸钙含量,某同学将鸡蛋壳洗净、充分干燥并捣碎,展开了下列探究:(1)将溶质质量分数为35%的浓盐酸配制成10%的稀盐酸,操作步骤为:
步骤1:计算所需浓盐酸和水的体积;
步骤2:根据计算结果,用量筒(填仪器名称)分别量取所需的浓盐酸和水;
步骤3:将浓盐酸倒入水中并用玻璃棒搅拌得到稀盐酸.
(2)测得各自的质量后,将鸡蛋壳置于如图所示的锥形瓶中,打开分液漏斗中的活塞,使其充分反应,直到不再产生气泡为止(假设装置中的稀盐酸足量,鸡蛋壳中的其他物质不与稀盐酸反应).实验数据记录如下表:
(CaCO3+2HCl=CaCl2+H2O+CO2↑)
| 反应前 | 鸡蛋壳的质量 | 16克 |
| 装置和稀盐酸的总质量 | 220克 | |
| 反应后 | 装置及其内容物的总质量 | 231.6克 |
分析 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据提供的数据和反应的化学方程式可以进行相关方面的计算.
解答 解:(1)根据计算结果,用量筒分别量取所需的浓盐酸和水.
故填:量筒.
(2)设碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x (16+220-231.6)g
$\frac{100}{x}$=$\frac{44}{(16+220-231.6)g}$,
x=10g,
则该鸡蛋壳中碳酸钙的质量分数为:$\frac{10g}{16g}$×l00%=62.5%,
答:该鸡蛋壳中碳酸钙的质量分数为62.5%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
9.下列说法中正确的是( )
| A. | 铅笔中含有铅这种物质,所以铅笔有毒 | |
| B. | 金刚石、石墨、C60都是碳的单质 | |
| C. | 空气中的CO2含量达到10%的时候,会导致人死亡,所以这是种一有毒的气体 | |
| D. | 某物质只含有碳元素,这种物质一定是纯净物 |
10.科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环(如图1所示).
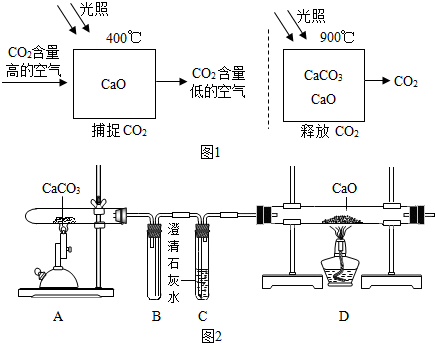
某化学小组的同学设计如图2装置探究上述设想的反应原理.
(1)能证明“释放CO2”的现象是C中澄清石灰水变浑浊.
(2)装置 B的作用是防止C中石灰水倒吸炸裂玻璃管.
(3)实验后小组同学对D中固体的成分进行探究.
[查阅资料]CaO+2HCl=CaCl2+H2O
[猜想与假设]D中的固体可能为①只有氧化钙;②氧化钙与碳酸钙; ③只有碳酸钙
[进行实验]

某化学小组的同学设计如图2装置探究上述设想的反应原理.
(1)能证明“释放CO2”的现象是C中澄清石灰水变浑浊.
(2)装置 B的作用是防止C中石灰水倒吸炸裂玻璃管.
(3)实验后小组同学对D中固体的成分进行探究.
[查阅资料]CaO+2HCl=CaCl2+H2O
[猜想与假设]D中的固体可能为①只有氧化钙;②氧化钙与碳酸钙; ③只有碳酸钙
[进行实验]
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量的D中固体于试管中,并加入一定量的水,振荡 | 触摸试管外壁,感觉发热,继续向试管中加入足量的稀盐酸,无气泡产生 | 猜想①正确 |
| 触摸试管外壁,感觉发热,继续向试管中加入足量的稀盐酸,有气泡产生 | 猜想②正确 | |
| 触摸试管外壁,温度不变,继续向试管中加入足量的稀盐酸,有气泡产生 | 猜想③正确 |
14.你正在质量检测考试,希望你仔细审题,细心答题,考出水平!你知道关于这次科学考试用的纸张的一些性质吗?请你分析下列性质中属于化学性质的是( )
| A. | 可燃 | B. | 不溶于水 | C. | 白色 | D. | 易撕碎 |
4.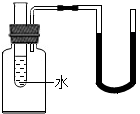 向右图试管里的水中加入下述某种物质后,原来U型管内在同一水平上的红墨水,右边液面降低左边液面上升,则加入的物质是( )
向右图试管里的水中加入下述某种物质后,原来U型管内在同一水平上的红墨水,右边液面降低左边液面上升,则加入的物质是( )
 向右图试管里的水中加入下述某种物质后,原来U型管内在同一水平上的红墨水,右边液面降低左边液面上升,则加入的物质是( )
向右图试管里的水中加入下述某种物质后,原来U型管内在同一水平上的红墨水,右边液面降低左边液面上升,则加入的物质是( )| A. | 硝酸铵 | B. | 氯化钠 | C. | 活性炭 | D. | 浓硫酸 |
8.化学是以实验为基础的自然科学,通过实验得出的下列结论不正确的是( )
| A. | 白磷可以在氧气中燃烧,说明氧气具有可燃性 | |
| B. | 1993年8月,我国科学家利用真空扫描隧道显微镜,在一块晶体硅的表面通过探针的作用搬走原子,写下了“中国”两 个字,这标志着我国科学已开始进入操 纵原子的阶段 | |
| C. | 把冷而干燥的小烧杯罩在蜡烛火焰的上方.小烧杯中有水雾生成,说明蜡烛中有氢元素 | |
| D. | 化合物是由不同种元素组成的.所以由不同元素组成的纯净物一定是化合物 |
10.(双项)从人类利用金属的历史来看,先是青铜器时代,而后是铁器时代,铝的利用是近百年的事.这个先后顺序跟下列因素有关的是( )
| A. | 地壳中金属元素的含量 | B. | 金属活动性顺序 | ||
| C. | 金属冶炼的难易程度 | D. | 金属的导电性 |
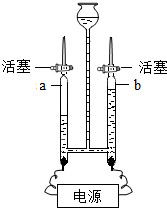 用如图装置进行水的电解实验.
用如图装置进行水的电解实验.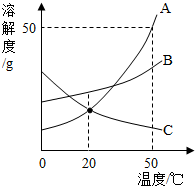 如图1所示,依据A、B、C三种固体物质的溶解度曲线,回答下列问题:
如图1所示,依据A、B、C三种固体物质的溶解度曲线,回答下列问题: