题目内容
12.某兴趣小组的同学为验证金属的化学性质,在实验室里将一小块黄铜(铜锌合金)放入烧杯中,加入一定量的稀硫酸,充分反应后过滤得固体和滤液.下列说法不正确的是( )| A. | 反应后溶液的质量一定大于反应前溶液质量 | |
| B. | 滤液中的溶质一定含有硫酸锌 | |
| C. | 滤液中的溶质一定不含有硫酸 | |
| D. | 反应后剩余的固体中一定含有铜 |
分析 铜不能和稀硫酸反应,锌和稀硫酸反应生成硫酸锌和氢气.
解答 解:A、锌和稀硫酸反应生成硫酸锌和氢气,随着反应的进行,溶液质量不断增大,该选项说法正确;
B、锌和稀硫酸反应生成硫酸锌和氢气,因此滤液中的溶质一定含有硫酸锌,该选项说法正确;
C、如果稀硫酸过量,则滤液中的溶质中含有硫酸,该选项说法不正确;
D、因为铜不能和稀硫酸反应,因此反应后剩余的固体中一定含有铜,该选项说法正确.
故选:C.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
2.下列关于物质的性质和用途说法不正确的是( )
| A. | 氮气充入食品中防腐,是利用氮气常温下化学性质稳定 | |
| B. | 氧气用于火箭发射,是利用氧气的可燃性 | |
| C. | 制作霓虹灯时充入稀有气体,是利用稀有气体通电能发出不同颜色的光 | |
| D. | 在冶铁工业中要用到一氧化碳,是利用了一氧化碳的还原性 |
3.如图是甲、乙两种固体物质的溶解度曲线图,下列说法正确的是( )


| A. | 甲、乙两物质的溶解度都随温度升高而增大 | |
| B. | 图中P点表示,甲、乙两种物质的溶解度相等 | |
| C. | t2℃时,将30 g 乙物质加入50 g水中,所得溶液的质量为80g | |
| D. | 在其他条件不变的情况下,若把t1℃时甲、乙的饱和溶液分别升温至t2℃,此时甲溶液中溶质的质量分数大于乙溶液 |
20.化学与生活息息相关,下列说法中,不合理的是( )
| A. | 室内洒水可防止煤气中毒 | B. | 稀有气体可用作电光源 | ||
| C. | 医用酒精可用于杀菌消毒 | D. | 干冰可用作环保制冷剂 |
17.某实验小组的四位同学在探究碱的性质时发现氢氧化钠、氢氧化钙等可溶性碱都能使酚酞试液变红.他们想进一步探究:不溶性的氢氧化镁是否也能使酚酞试液变红.为此,他们将适量的氢氧化镁加入到盛有热水的烧杯中搅拌,然后向浑浊的液体中滴加酚酞试液,发现酚酞试液变红,可是过一会儿红色又消失了.四位同学依据所学的化学知识,分别对上述酚酞试液变红、红色又消失的原因作了如下猜想:
小明:可能是个偶然现象.
小东:可能是浑浊液体中的固体氢氧化镁使酚酞试液变红,氢氧化镁沉降后溶液就变无色了.
小花:可能是酚酞试液与空气中的氧气反应,使红色消失;也可能是氢氧化镁溶液与空气中的二氧化碳反应的缘故.
小红:可能是在热水中氢氧化镁的溶解度大,溶液中OH-离子较多,使酚酞试液变红;过一会儿温度降低,氢氧化镁的溶解度减小,溶液中OH-离子变少,酚酞试液又变无色.
(1)对小明猜想“是个偶然现象”,四位同学都认为可以用科学探究的一般方法排除偶然现象.他们的方法是:重复实验.
(2)小花认为小东的猜想不正确,她从碱使酚酞试液变色的原因上给予了否定,小花的理由是固体氢氧化镁中没有自由移动的氢氧根离子,不能使酚酞试液变红.
(3)四位同学讨论后认为要验证小花的猜想,还需做如下实验,你知道其实验的目的吗?
(4)对小红的猜想,实验小组的同学设计了多种实验方案进行证明,其中一种如下表.
小明:可能是个偶然现象.
小东:可能是浑浊液体中的固体氢氧化镁使酚酞试液变红,氢氧化镁沉降后溶液就变无色了.
小花:可能是酚酞试液与空气中的氧气反应,使红色消失;也可能是氢氧化镁溶液与空气中的二氧化碳反应的缘故.
小红:可能是在热水中氢氧化镁的溶解度大,溶液中OH-离子较多,使酚酞试液变红;过一会儿温度降低,氢氧化镁的溶解度减小,溶液中OH-离子变少,酚酞试液又变无色.
(1)对小明猜想“是个偶然现象”,四位同学都认为可以用科学探究的一般方法排除偶然现象.他们的方法是:重复实验.
(2)小花认为小东的猜想不正确,她从碱使酚酞试液变色的原因上给予了否定,小花的理由是固体氢氧化镁中没有自由移动的氢氧根离子,不能使酚酞试液变红.
(3)四位同学讨论后认为要验证小花的猜想,还需做如下实验,你知道其实验的目的吗?
| 实验步骤 | 设计目的 |
| 将氢氧化镁加入到热水中搅拌,滴入酚酞试液,并在上方滴一些植物油. |
| 实验方法 | 可能观察到的现象 | 相应结果或结论 |
| 取两支试管,分别加入相同质量的氢氧化镁和相同质量的热水振荡,各滴加数滴酚酞试液.一支保持温度不变,另一支自然冷却. | 保持温度不变的红色不消失,自然冷却的红色消失. |
4.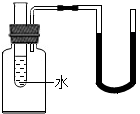 向右图试管里的水中加入下述某种物质后,原来U型管内在同一水平上的红墨水,右边液面降低左边液面上升,则加入的物质是( )
向右图试管里的水中加入下述某种物质后,原来U型管内在同一水平上的红墨水,右边液面降低左边液面上升,则加入的物质是( )
 向右图试管里的水中加入下述某种物质后,原来U型管内在同一水平上的红墨水,右边液面降低左边液面上升,则加入的物质是( )
向右图试管里的水中加入下述某种物质后,原来U型管内在同一水平上的红墨水,右边液面降低左边液面上升,则加入的物质是( )| A. | 硝酸铵 | B. | 氯化钠 | C. | 活性炭 | D. | 浓硫酸 |
1.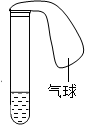 如图所示:试管中盛有某种液体,将气球中的某种固体小心地倒入试管中.下列各组物质中,不能使气球逐渐变大的是( )
如图所示:试管中盛有某种液体,将气球中的某种固体小心地倒入试管中.下列各组物质中,不能使气球逐渐变大的是( )
 如图所示:试管中盛有某种液体,将气球中的某种固体小心地倒入试管中.下列各组物质中,不能使气球逐渐变大的是( )
如图所示:试管中盛有某种液体,将气球中的某种固体小心地倒入试管中.下列各组物质中,不能使气球逐渐变大的是( )| A. | 铁粉和稀硫酸 | B. | 氯化钠和水 | C. | 镁和稀硫酸 | D. | 石灰石和稀盐酸 |
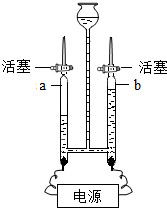 用如图装置进行水的电解实验.
用如图装置进行水的电解实验.