题目内容
1.日常生活离不开化学.(1)长期盛装澄清石灰水的试剂瓶壁,常出现“白膜”,其形成的原因是(用化学方程式表示)CO2+Ca(OH)2═CaCO3↓+H2O,该“白膜”可用稀盐酸清洗,反应原理是(用化学方程式表示)CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)配制果味饮料发生如下反应,请将反应的化学方程式补充完整.
3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3CO2↑
分析 (1)根据石灰水能与空气中的二氧化碳反应生成碳酸钙白色沉淀;碳酸钙难溶于水,能与酸反应,可用稀盐酸洗去;进行分析解答.
(2)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物的化学式.
解答 解:(1)二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水,使石灰水的表面形成一层白膜,这层白膜的成分主要是碳酸钙,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
碳酸钙难溶于水,能与酸反应,实验室洗涤该试剂瓶可用稀盐酸洗去,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
故答案为:CO2+Ca(OH)2═CaCO3↓+H2O;稀盐酸;CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)根据反应的化学方程式,反应物中钠、氢、碳、氧原子个数分别为3、9、11、16,反应后的生成物中钠、氢、碳、氧原子个数分别为3、5、9、13,根据反应前后原子种类、数目不变,则未知物质中含有6个氢原子和3个氧原子,则横线上物质的化学式为3H2O.故填:3H2O.
点评 本题难度不大,掌握二氧化碳的化学性质和质量守恒定律并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
11.南海、钓鱼岛及其附属海域是我国固有领土,蕴藏着丰富的海洋资源.
(1)海水制盐.从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质.为得到较纯的氯化钠,将粗盐溶于水,然后进行如下操作:a.加过量的Ba(OH)2溶液;b.加稍过量的盐酸;c.加过量的Na2CO3溶液;d.过滤;e.蒸发.正确的操作顺序是acdbe(填字母).加Na2CO3溶液的作用是除去氯化钙和过量试剂氢氧化钡.
(2)海水淡化.图1是一个简易的蒸馏法淡化海水的装置.证明得到的水是淡水的最简便方法是蒸干后没有晶体析出.

(3)海水制镁.浓海水中主要离子的浓度如上表.从浓海水中提取金属镁的一段工艺流程如图2所示:
写出反应1的化学方程式:Ca(OH)2+MgCl2=CaCl2+Mg(OH)2↓.滤液X中溶质的主要成分有CaCl2、NaCl(填化学式).将MgCl2溶液在一定条件下蒸发结晶、熔融电解可制得金属镁.则2L浓海水理论上可得到金属镁的质量为57.6g.
(4)海水“制碱”.氨碱法制纯碱是先向饱和食盐水通入氨气、二氧化碳生成NaHCO3和NH4Cl,NaHCO3结晶析出,再加热NaHCO3制得纯碱.写出生成NaHCO3和NH4Cl的化学方程式为NH3+CO2+NaCl+H2O=NaHCO3+NH4Cl;反应中生成NaHCO3和NH4Cl的质量比为84:53.5,NaHCO3和NH4Cl的溶解度曲线如图3所示.请分析NaHCO3结晶析出而NH4Cl没有结晶析出的原因是生成的NaHCO3质量比NH4Cl多而溶解度比NH4Cl小,先达到饱和.
(1)海水制盐.从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质.为得到较纯的氯化钠,将粗盐溶于水,然后进行如下操作:a.加过量的Ba(OH)2溶液;b.加稍过量的盐酸;c.加过量的Na2CO3溶液;d.过滤;e.蒸发.正确的操作顺序是acdbe(填字母).加Na2CO3溶液的作用是除去氯化钙和过量试剂氢氧化钡.
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/g/L | 63.7 | 28.8 | 144.6 | 46.4 |

(3)海水制镁.浓海水中主要离子的浓度如上表.从浓海水中提取金属镁的一段工艺流程如图2所示:
写出反应1的化学方程式:Ca(OH)2+MgCl2=CaCl2+Mg(OH)2↓.滤液X中溶质的主要成分有CaCl2、NaCl(填化学式).将MgCl2溶液在一定条件下蒸发结晶、熔融电解可制得金属镁.则2L浓海水理论上可得到金属镁的质量为57.6g.
(4)海水“制碱”.氨碱法制纯碱是先向饱和食盐水通入氨气、二氧化碳生成NaHCO3和NH4Cl,NaHCO3结晶析出,再加热NaHCO3制得纯碱.写出生成NaHCO3和NH4Cl的化学方程式为NH3+CO2+NaCl+H2O=NaHCO3+NH4Cl;反应中生成NaHCO3和NH4Cl的质量比为84:53.5,NaHCO3和NH4Cl的溶解度曲线如图3所示.请分析NaHCO3结晶析出而NH4Cl没有结晶析出的原因是生成的NaHCO3质量比NH4Cl多而溶解度比NH4Cl小,先达到饱和.
12.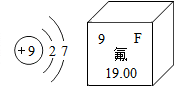 某元素原子结构示意图及在元素周期表中的相关信息如图所示,下列说法正确的是( )
某元素原子结构示意图及在元素周期表中的相关信息如图所示,下列说法正确的是( )
 某元素原子结构示意图及在元素周期表中的相关信息如图所示,下列说法正确的是( )
某元素原子结构示意图及在元素周期表中的相关信息如图所示,下列说法正确的是( )| A. | 该元素的名称为F | |
| B. | 该元素的原子序数为9 | |
| C. | 该元素的相对原子质量为19 | |
| D. | 该元素原子在化学反应中容易失去电子变为阳离子 |
6.下列符号与其叙述对应一致的是( )
| A. | 3H--3个氢元素 | |
| B. | C60--60个碳原子 | |
| C. | ${\stackrel{+3}{AI}}_{\;}$2O3--氧化铝中铝元素的化合价为+3价 | |
| D. | NaCl2--氯化钠 |
13.下列变化中,属于化学变化的是( )
| A. | 石油的蒸馏 | B. | 米酿成酒 | C. | 汽油的挥发 | D. | 干冰的升华 |
 铝元素与人类关系密切.
铝元素与人类关系密切.