题目内容
12.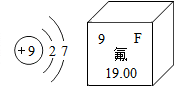 某元素原子结构示意图及在元素周期表中的相关信息如图所示,下列说法正确的是( )
某元素原子结构示意图及在元素周期表中的相关信息如图所示,下列说法正确的是( )| A. | 该元素的名称为F | |
| B. | 该元素的原子序数为9 | |
| C. | 该元素的相对原子质量为19 | |
| D. | 该元素原子在化学反应中容易失去电子变为阳离子 |
分析 根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量;若原子的最外层电子数为8,则为稀有气体元素,属于相对稳定结构;若最外层电子数≥4,则一般为非金属元素,在化学反应中易得电子,若最外层电子数<4,则一般为金属元素,在化学反应中易失去电子;进行分析判断即可.
解答 解:A、根据元素周期表中的一格中获取的信息,该元素的名称是氟,元素符号为F,故选项说法错误.
B、根据元素周期表中的一格中获取的信息,该元素的原子序数为9,故选项说法正确.
C、根据元素周期表中的一格中获取的信息,该元素原子的相对原子质量为19.00,故选项说法错误.
D、氟原子最外层电子数为7,在化学反应过程中该元素原子容易得到1个电子形成阴离子,故选项说法错误.
故选:B.
点评 本题考查学生对元素周期表的理解及对原子结构示意图的认识,清楚每部分所表达的含义,即可解答.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
10.2016年5月,“感知环境,智慧环保”无锡环境监控物联网应用示范工程进入整体试运行阶段,下列做法不利于环境质量提升的是( )
| A. | 对污染水体作处理使之符合排放标准 | |
| B. | 应用新技术、新工艺减少污染物的产生 | |
| C. | 加大汽车尾气检测力度,减少空气污染 | |
| D. | 减少使用农家肥,大量使用化肥和农药 |
20.为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,同学们通过测定了反应后溶液的pH,得到了如图所示的pH曲线,请回答:
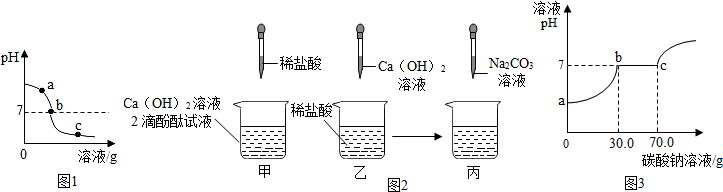
(1)由图1可知该实验操作是将稀盐酸滴加到另一种溶液中;
(2)该反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;
(3)实验过程中,取a、b、c三处反应后的溶液于三个烧杯中,但是忘了做标记,同学们通过设计方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液.
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3═CaCO3↓+2NaCl.
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现溶液由无色变成红色的现象.结论:该样品是a处溶液.
②为进一步确定b或c处溶液,又设计了如表方案:
(4)如图2,同学们做甲、乙、两个中和反应实验的探究.
①甲实验恰好中和,则该溶液中的溶质是CaCl2(化学式).
②取乙反应后的溶液60.0g,滴加质量分数26.5%的Na2CO3溶液,如图2丙,溶液pH的变化如图3,请计算该溶液中CaCl2的溶质质量分数18.5%(写出计算过程,精确到0.1%).

(1)由图1可知该实验操作是将稀盐酸滴加到另一种溶液中;
(2)该反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;
(3)实验过程中,取a、b、c三处反应后的溶液于三个烧杯中,但是忘了做标记,同学们通过设计方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液.
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3═CaCO3↓+2NaCl.
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现溶液由无色变成红色的现象.结论:该样品是a处溶液.
②为进一步确定b或c处溶液,又设计了如表方案:
| 实验步骤 | 实验现象 | 实验结论 |
| 另取余下样品少量于两支试管中,分别滴加足量的Na2CO3溶液. | ①只产生白色沉淀 | 该样品为b处溶液. |
| ②先产生气泡,后产生白色沉淀 | 该样品为c处溶液,并推知溶液中的阳离子有Ca2+、H+ |
①甲实验恰好中和,则该溶液中的溶质是CaCl2(化学式).
②取乙反应后的溶液60.0g,滴加质量分数26.5%的Na2CO3溶液,如图2丙,溶液pH的变化如图3,请计算该溶液中CaCl2的溶质质量分数18.5%(写出计算过程,精确到0.1%).
17.某品牌谷物牛奶饮品营养成分表数据显示:每250mL含钠78mg、磷78mg、钾91mg、钙91mg.这里的钠、磷、钾、钙是指( )
| A. | 单质 | B. | 分子 | C. | 元素 | D. | 氧化物 |
2.除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是( )
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | CO2(CO) | 氧气 | 点燃 |
| B | MnO2(KCl) | 水 | 溶解、过滤 |
| C | NH3(H2O) | 足量的浓H2SO4 | 洗气 |
| D | CuO(Cu) | 适量的稀盐酸 | 过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
 已知A~F六种物质均为初中化学常见物质,其中B、E为氧化物,A、B、D、F为不同类别的化合物,A、B、D分别放入水中都能使酚酞溶液变红,如图是它们之间的关系(部分反应物和产物已省略;“→”表示转化,“-”表示相互反应).
已知A~F六种物质均为初中化学常见物质,其中B、E为氧化物,A、B、D、F为不同类别的化合物,A、B、D分别放入水中都能使酚酞溶液变红,如图是它们之间的关系(部分反应物和产物已省略;“→”表示转化,“-”表示相互反应).