题目内容
1. 已知:A、B、C、D是中学化学常见的物质,其中A、C为化合物,B、D为单质,它们之间能够发生如下反应:
已知:A、B、C、D是中学化学常见的物质,其中A、C为化合物,B、D为单质,它们之间能够发生如下反应:请回答:
(1)若D为密度最小的气体,请写出一个符合要求的化学方程式,并指出实验室收集D气体的方法.
(2)若A为黑色固体,C为使石灰水变浑浊的气体,请写出一个符合要求的化学方程式,并指出B的一种用途.
分析 由已知条件可以知道需要写的化学反应都属于置换反应;根据反应物和生成物的要求结合已知的反应分析合理的反应,书写化学方程式时,必须熟悉反应物、生成物和反应条件,必须遵循质量守恒定律的两个原则.
解答 解:(1)A、C为化合物,B、D为单质,且D为密度最小的气体,则D为氢气,因此该置换反应可以是活泼金属和酸反应产生氢气和盐的反应,如锌与硫酸反应生成硫酸锌和氢气,该反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;因为氢气的密度比空气小,不易溶于水,因此可以采用向下排空气法或排水法收集;故答案为:Zn+H2SO4=ZnSO4+H2↑(合理即可);向下排空气法或排水法;
(2)A为黑色固体,C为使石灰水变浑浊的气体,即C是二氧化碳,可以是碳、氢气还原氧化铜生成铜和二氧化碳的反应,反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑或H2+2CuO$\frac{\underline{\;高温\;}}{\;}$Cu+H2O;其中的一氧化碳和氢气可以用作燃料、冶炼金属等;
故答案为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑或H2+2CuO$\frac{\underline{\;高温\;}}{\;}$Cu+H2O;用作燃料、冶炼金属等.
点评 本题主要考查化学方程式的书写和置换反应的判断和应用,难度不大,解题的关键是熟练掌握常见的反应并分析反应的特点找出合适的反应.

练习册系列答案
相关题目
11.关于溶液的下列说法正确的是( )
| A. | 常温下将100mL饱和Ca(OH)2溶液加热到50℃会变为不饱和溶液 | |
| B. | 从浓度为25%的H2SO4溶液中取出10mL,剩余溶液浓度仍为25% | |
| C. | 20℃时,50克水中溶解了18克NaCl,则20℃时NaCl的溶解度为36克 | |
| D. | 将95克KCl溶液蒸干得到5克固体,则原溶液中KCl的质量分数为5% |
9.关于反映3Cu+8HNO3(稀)═3Cu(NO3)2+2X↑+4H2O,下列说法不正确的是( )
| A. | X的化学式为H2 | |
| B. | 铜的化合价由0升至+2 | |
| C. | 可采用与制取CO2相同的发生装置制取X | |
| D. | 该反应涉及的物质中,构成粒子有原子、分子、离子 |
13.下列物质溶于水,溶液温度明显降低的是( )
| A. | 硝酸铵 | B. | 浓硫酸 | C. | 氢氧化钠 | D. | 氯化钠 |
10.有一包白色粉末,可能是由硫酸铜、氯化钠、碳酸钠、硫酸钠中的一种或几种组成.为检验其中的成分,某同学经实验得到下表,其中由实验及实验现象得出的结论不正确的是( )
| 实验步骤及现象 | 结论 | |
| A | ①将少许白色粉末溶于水,得到无色溶液甲 | 白色粉末中一定没有硫酸铜 |
| B | ②在甲中加足量氯化钡溶液,生成白色沉淀乙;过滤得滤液丙 | 白色粉末中可能有碳酸钠、硫酸钠 |
| C | ③在白色沉淀乙中加足量稀硝酸,沉淀部分溶解 | 白色粉末中一定含有硫酸钠和碳酸钠 |
| D | ④在滤液丙中,加入硝酸银溶液,出现白色沉淀 | 白色粉末中一定有氯化钠 |
| A. | A | B. | B | C. | C | D. | D |
11.硫酸锌可作为食品锌强化剂的原料.工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3、MgO等,工艺流程图如下:
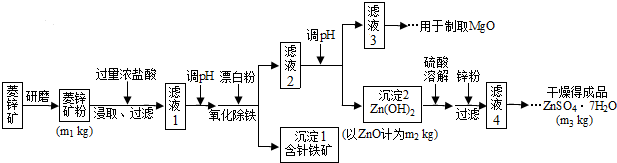
【查阅资料】①一般情况下,难溶性碱受热易分解,生成对应的金属氧化物和水;
②Mg(OH)2和Zn(OH)2开始沉淀和沉淀完全时的pH如下表所示:
根据上图回答下列问题:
(1)将菱锌矿研磨成粉的目的是增大反应物之间的接触面积,加快反应速率或使反应更充分;
(2)针铁矿的组成元素是Fe、O和H,相对分子质量是89,针铁矿中铁原子数:氧原子数:氢原子数=1:2:1;(提示:氢原子数目小于氧原子数目)
(3)“滤液4”之前加入锌粉的目的是除去过量的稀硫酸;
(4)工业上从“滤液3”制取MgO过程中,合适的反应物是bd(选填序号);
a.大理石粉 b.石灰乳 c.纯碱溶液 d.烧碱溶液
(5)完成这个流程中发生的化学反应方程式:
4Fe(OH)2+Ca(ClO)2+2H2O=4Fe(OH)3+CaCl2.

【查阅资料】①一般情况下,难溶性碱受热易分解,生成对应的金属氧化物和水;
②Mg(OH)2和Zn(OH)2开始沉淀和沉淀完全时的pH如下表所示:
| Mg(OH)2 | Zn(OH)2 | |
| 开始沉淀的pH | 10.4 | 6.4 |
| 沉淀完全的pH | 12.4 | 8.0 |
| 开始溶解的pH | -- | 10.5 |
(1)将菱锌矿研磨成粉的目的是增大反应物之间的接触面积,加快反应速率或使反应更充分;
(2)针铁矿的组成元素是Fe、O和H,相对分子质量是89,针铁矿中铁原子数:氧原子数:氢原子数=1:2:1;(提示:氢原子数目小于氧原子数目)
(3)“滤液4”之前加入锌粉的目的是除去过量的稀硫酸;
(4)工业上从“滤液3”制取MgO过程中,合适的反应物是bd(选填序号);
a.大理石粉 b.石灰乳 c.纯碱溶液 d.烧碱溶液
(5)完成这个流程中发生的化学反应方程式:
4Fe(OH)2+Ca(ClO)2+2H2O=4Fe(OH)3+CaCl2.

 如图是实验室常用的制取气体的装置.
如图是实验室常用的制取气体的装置.