题目内容
下面是工厂苛化法生产烧碱的示意图.
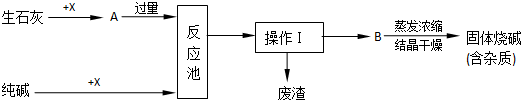
(1)在实验室,操作Ⅰ的名称是 ;经操作Ⅰ得到废渣的主要成份是 (写化学式).
(2)物质X中各元素的质量比表示为 .
(3)某工厂化验员向含有1.6g氢氧化钠的溶液中,逐滴加入20.0g盐酸至氢氧化钠和盐酸恰好完全反应.求盐酸中溶质的质量分数为多少?(写出过程)
(4)若用1.6g上述得到的固体烧碱产品(含杂质)代替1.6g氢氧化钠,逐滴加入上述相同浓度盐酸至反应物恰好完全反应,则消耗盐酸的质量 20g(填“大于”、“等于”或“小于”).

(1)在实验室,操作Ⅰ的名称是
(2)物质X中各元素的质量比表示为
(3)某工厂化验员向含有1.6g氢氧化钠的溶液中,逐滴加入20.0g盐酸至氢氧化钠和盐酸恰好完全反应.求盐酸中溶质的质量分数为多少?(写出过程)
(4)若用1.6g上述得到的固体烧碱产品(含杂质)代替1.6g氢氧化钠,逐滴加入上述相同浓度盐酸至反应物恰好完全反应,则消耗盐酸的质量
考点:物质的相互转化和制备,过滤的原理、方法及其应用,有关溶质质量分数的简单计算,生石灰的性质与用途,盐的化学性质,根据化学反应方程式的计算
专题:物质的制备
分析:由图示的过程可知利用氧化钙和纯碱制取氢氧化钙的过程是:氧化钙与水反应生成氢氧化钙,氢氧化钙再与碳酸钠反应生成碳酸钙和氢氧化钠,过滤得氢氧化钠的溶液,进行蒸发操作后可得氢氧化钠固体,据此对过程进行分析判断即可.
解答:解:
(1)由于氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,操作Ⅰ将固体与液体分开,因此为过滤,所以废渣的主要成份是碳酸钙;
(2)纯碱属于盐,制取烧碱必须是碱和盐反应生成新碱和新盐,需要用氧化钙制取碱,氧化钙与水反应生成氢氧化钙,所以X是水,化学式为H2O;水中氢氧元素的质量比为2:16=1:8
(3)设与氢氧化钠反应消耗氯化氢的质量为x,则:
NaOH+HCl═NaCl+H2O
40 36.5
1.6g x
40:36.5═1.6 g:x
x=
=1.46 g
盐酸中溶质的质量分数为
×100%=7.3%
由图示可知A物质是过量,所以氢氧化钙是过量的,滤液中会混有氢氧化钙.
设与1.6g氢氧化钙反应消耗掉氯化氢质量为y
Ca(OH)2+2HCl═CaCl2+2H2O
74 73
1.6g y
则
=
,解得y=1.58g
盐酸的质量为
=21.6g>20g
因此用上述得到的固体烧碱产品(含氢氧化钙)代替1.6g氢氧化钠,逐滴加入上述相同浓度盐酸至反应物恰好完全反应,则消耗盐酸的质量大于20g
故答案为:
(1)过滤; CaCO3.(2)1:8 (3)7.3%,大于
(1)由于氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,操作Ⅰ将固体与液体分开,因此为过滤,所以废渣的主要成份是碳酸钙;
(2)纯碱属于盐,制取烧碱必须是碱和盐反应生成新碱和新盐,需要用氧化钙制取碱,氧化钙与水反应生成氢氧化钙,所以X是水,化学式为H2O;水中氢氧元素的质量比为2:16=1:8
(3)设与氢氧化钠反应消耗氯化氢的质量为x,则:
NaOH+HCl═NaCl+H2O
40 36.5
1.6g x
40:36.5═1.6 g:x
x=
| 1.6g×36.5 |
| 40 |
盐酸中溶质的质量分数为
| 1.46g |
| 20.0g |
由图示可知A物质是过量,所以氢氧化钙是过量的,滤液中会混有氢氧化钙.
设与1.6g氢氧化钙反应消耗掉氯化氢质量为y
Ca(OH)2+2HCl═CaCl2+2H2O
74 73
1.6g y
则
| 74 |
| 1.6g |
| 73 |
| y |
盐酸的质量为
| 1.58g |
| 7.3% |
因此用上述得到的固体烧碱产品(含氢氧化钙)代替1.6g氢氧化钠,逐滴加入上述相同浓度盐酸至反应物恰好完全反应,则消耗盐酸的质量大于20g
故答案为:
(1)过滤; CaCO3.(2)1:8 (3)7.3%,大于
点评:此题是一道框题推断分析题,其主干就是工业上制取烧碱的方法,只要能依据氢氧化钠是由碳酸钠和氢氧化钙制取的原理进行分析,即可得相应的问题答案.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目

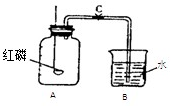 某学生为验证空气中氧气的体积分数进行了如下实验(如图所示).燃烧匙里盛燃着的足量的红磷,反应结束,冷却后,打开C夹,水沿导管进入A瓶.
某学生为验证空气中氧气的体积分数进行了如下实验(如图所示).燃烧匙里盛燃着的足量的红磷,反应结束,冷却后,打开C夹,水沿导管进入A瓶. 如图是甲、乙、丙三种固体物质的溶解度曲线.请回答:
如图是甲、乙、丙三种固体物质的溶解度曲线.请回答: