题目内容
10.用化学符号表示(1)2个氧分子2O2
(2)1个锌原子Zn;
(3)三个硫酸根离子3SO42-
(4)某物质由O、N两种元素组成,其中N的化合价为+1,该物质的化学式是Na2O.
分析 (1)分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字.
(2)原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
(3)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.
(4)某物质由O、N两种元素组成,其中N的化合价为+1,氧元素显-2价,其化学式即可.
解答 解:(1)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则2个氧分子可表示为:2O2.
(2)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故1个锌原子表示为:Zn.
(3)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故3个硫酸根离子可表示为:3SO42-.
(4)某物质由O、N两种元素组成,其中N的化合价为+1,氧元素显-2价,化学式为Na2O.
故答案为:(1)2O2;(2)Zn;(3)3SO42-;(4)Na2O.
点评 本题难度不大,掌握常见化学用语(原子符号、分子符号、化学式、离子符号等)的书写方法是正确解答此类题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1. 用“○”和“●”分别代表A、B两种原子,如图所示,单质A2与单质B2在一定条件下能发生化学反应生成新物质X.下列说法正确的是( )
用“○”和“●”分别代表A、B两种原子,如图所示,单质A2与单质B2在一定条件下能发生化学反应生成新物质X.下列说法正确的是( )
 用“○”和“●”分别代表A、B两种原子,如图所示,单质A2与单质B2在一定条件下能发生化学反应生成新物质X.下列说法正确的是( )
用“○”和“●”分别代表A、B两种原子,如图所示,单质A2与单质B2在一定条件下能发生化学反应生成新物质X.下列说法正确的是( )| A. | 在反应过程中A2和B2分子保持不变 | |
| B. | 该反应为置换反应 | |
| C. | 参加反应的A2与B2分子数之比为3:1 | |
| D. | 物质X含三种元素 |
18.下列图示与对应的叙述不相符的是( )
| A. | 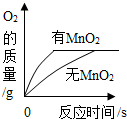 探究双氧水制氧气中MnO2的作用 探究双氧水制氧气中MnO2的作用 | |
| B. |  将水通电电解一段时间后的气体体积变化 将水通电电解一段时间后的气体体积变化 | |
| C. | 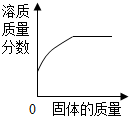 20℃时向不饱和KNO3溶液中继续加KNO3后溶质质量分数变化 20℃时向不饱和KNO3溶液中继续加KNO3后溶质质量分数变化 | |
| D. |  向两份完全相同的盐酸中分别加入足量锌粉、镁粉 向两份完全相同的盐酸中分别加入足量锌粉、镁粉 |
5.在氧气中燃烧,会产生浓厚白烟的是( )
| A. | 红磷 | B. | 木炭 | C. | 硫磺 | D. | 铁丝 |
2.生活中常遇见铜制品生锈的情况.活动课上,同学们设计实验对铜锈进行了如下探究活动.

探究活动一:验证铜锈的组成
【査阅资料】①铜锈为绿色,其主要成分是Cu2(OH)2CO3.②白色的硫酸铜粉末遇水能变为蓝色.③碳不与稀硫酸反应.④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
【进行实验1】同学们设计了如图所示装置并进行实验.
【进行实验2】同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显.

探究活动一:验证铜锈的组成
【査阅资料】①铜锈为绿色,其主要成分是Cu2(OH)2CO3.②白色的硫酸铜粉末遇水能变为蓝色.③碳不与稀硫酸反应.④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
【进行实验1】同学们设计了如图所示装置并进行实验.
| 实验橾作 | 实验现象 | 实验结论 |
| ①按如图组装仪器,装入药品. ②加热铜锈,直至不再有气体产生,停止加热. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有 CO2、H2O、CuO;铜绣由Cu、C、H、O元素组成;烧杯中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O. |
| ③冷却后,向试管中固体 加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变 为蓝色. |
| 序号 | 实验内容 | 实验结论 | 实验反思 |
| 实验1 | 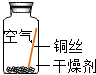 | 在干燥环境中,铜不易生锈 | (1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是 除去蒸馏水中溶解的O2和CO2. (2)如果要证明铜生锈的快慢是否与二氧化碳的浓度有关,还需要补充的一个实验内容是 按实验4内容重复操作后,再通入一定量的CO2排出部分空气,塞紧胶塞. |
| 实验2 | 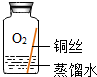 | 在有O2和H2O、无CO2的环境中,铜不易生锈 | |
| 实验3 | 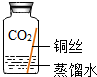 | 在有CO2和H2O、无O2的环境中,铜不易生锈 | |
| 实验4 | 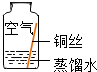 | 铜生锈的条件是 与O2、CO2和H2O同时接触 |
19.有pH=4的稀硫酸溶液,要使它的pH升高,下列方法中不可能实现的是( )
| A. | 加入氢氧化钠溶液 | B. | 加入大量的硫酸钠溶液 | ||
| C. | 加入一定量的铁粉 | D. | 加入硝酸钡固体 |
 我国海岸线长达3.2万千米,海洋专属经济区幅员辽阔,海洋资源丰富,开发的前景十分远大.
我国海岸线长达3.2万千米,海洋专属经济区幅员辽阔,海洋资源丰富,开发的前景十分远大.

