题目内容
为防控H7N9病毒,一定要定时对畜禽栏舍进行消毒.在农村,生石灰也常用于畜禽栏舍的消毒.畜禽出栏后,将生石灰用水调成20%的石灰乳,涂刷墙面和地面.某农户误将生石灰直接撒在猪圈中消毒,一段时间后发现猪的蹄部干燥开开裂,有的甚至出现灼伤、溃疡,原因是 .上述用于消毒的浆状物要现配现用,放过久就没有消毒作用了,原因是 (用化学方程式表示).
考点:生石灰的性质与用途,碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的碱 碱的通性
分析:根据氧化钙的性质进行分析,氧化钙能与水反应放出大量的热,生成的氢氧化钙具有消毒的性质,氢氧化钙能与二氧化碳反应生成碳酸钙和水解答.
解答:解:氧化钙能与水反应放出大量的热,生成的氢氧化钙具有腐蚀性,而导致猪的蹄部干燥开裂,有的甚至出现灼伤、溃疡,故填:生石灰与水反应放出大量的热且生成的氢氧化钙具有腐蚀性;
氢氧化钙能与空气中的二氧化碳反应生成碳酸钙和水而失去消毒的作用,故填:Ca(OH)2+CO2═CaCO3↓+H2O;
答案:生石灰与水反应放出大量的热且生成的氢氧化钙具有腐蚀性;Ca(OH)2+CO2═CaCO3↓+H2O
氢氧化钙能与空气中的二氧化碳反应生成碳酸钙和水而失去消毒的作用,故填:Ca(OH)2+CO2═CaCO3↓+H2O;
答案:生石灰与水反应放出大量的热且生成的氢氧化钙具有腐蚀性;Ca(OH)2+CO2═CaCO3↓+H2O
点评:本题考查了氧化钙的用途,完成此题,可以依据氧化钙的性质进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
点燃10g氢气和氧气的混合气体,爆炸后生成了4.5g的水,则原混合气体中氢气和氧气的质量比为( )
| A、1:19 | B、1:9 |
| C、3:2 | D、1:1 |
下列关于资源的叙述正确的是( )
| A、金属的回收利用不仅可以节约金属资源和能源,还可以减少对环境的污染 |
| B、海洋中含量最多的物质是氯化钠 |
| C、总投资5000亿的南水北调工程,有东线、中线和西线三条调水线路.是把中国汉江流域 丰盈的水资源抽调一部分送到华北和西北地区.从而改变中国南涝北旱和北方地区水资源严重短缺局面的重大战略性工程 |
| D、空气是一种重要的自然资源,它是由氧气和氮气两种气体组成的 |
现有100g质量分数为10%的硝酸钾溶液,要使它的质量分数增大一倍(此时溶液仍未达到饱和),可以采用的方法有( )
| A、溶剂蒸发掉一半 |
| B、溶剂蒸发掉50g |
| C、再加入10g溶质 |
| D、再加入12.5g溶质 |
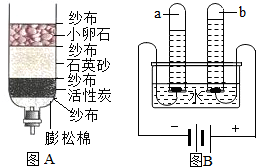 (1)向盛有水的烧杯中加入少量品红,静置一段时间后,溶液逐渐变成红色,此实验主要说明分子的性质是
(1)向盛有水的烧杯中加入少量品红,静置一段时间后,溶液逐渐变成红色,此实验主要说明分子的性质是