题目内容
2.某研究性学习小组对中和反应进行探究.实验1 验证酸与碱能发生中和反应.
进行如图1所示实验.

①实验中,能证明酸与碱发生中和反应的现象
是滴有酚酞的NaOH溶液褪色,发生反应的化学方程式为NaOH+HClNaCl+H2O.
实验2 证明酸与碱反应有水生成.
查阅资料:变色硅胶吸水后由蓝色变红色;无水醋酸常温下为无色液体;无水醋酸和氢氧化钠固体混合后生成醋酸钠和水.
实验探究:如图2所示,分别往4支试管中装入对应的试剂,迅速塞紧橡胶塞.实验过程中,A、B和C试管中均无明显现象.
②迅速塞紧橡胶塞的目的是避免空气中的水蒸气对实验造成干扰.
③设置A、B、C实验的目的是证明中和反应中若没有水生成,硅胶不变色(或对比实验等合理答案).
④能证明酸与碱反应有水生成的实验现象是试管D中硅胶由蓝色变为红色,试管A、B、C中硅胶不变色.
分析 ①根据酚酞在酸、碱溶液中的颜色的变化分析;
②根据空气的成分分析;
③通过实验对比,硅胶颜色的变化分析;
④根据硅胶的颜色的变化分析反应是否有有水生成.
解答 解:①无色酚酞试液在氢氧化钠溶液中显红色,滴入了稀盐酸变成了无色,说明了盐酸与氢氧化钠发生了反应;反应的方程式为:NaOH+HCl=NaCl+H2O;
②空气中含有水,也能使硅胶变色,迅速塞紧橡胶塞可防止空气中的水分进入试管干扰试验;
③通过实验ABC的实验现象的对比证明了无水醋酸和氢氧化钠、醋酸钠固体都不含有水,不能使硅胶变色,由试验D硅胶的变色说明了中和反应有水生成.
④能证明酸和碱反应有水生成的现象是:试管D中硅胶由蓝色变为红色,试管A、B、C中硅胶不变色;
故答案为:①滴有酚酞的NaOH溶液褪色;NaOH+HCl=NaCl+H2O;②水蒸气;③证明中和反应中若没有水生成,硅胶不变色(或对比实验等合理答案); ④试管D中硅胶由蓝色变为红色,试管A、B、C中硅胶不变色.
点评 本题属于实验探究题,综合性较强,只有综合掌握了基础知识才能较好的完成本类练习题.

练习册系列答案
相关题目
12.关于油脂的下列说法错误的是( )
| A. | 蛋白质、糖类、油脂中,单体质量时油脂所能提供的热量最多 | |
| B. | 油脂是维持生命活动的备用能源 | |
| C. | 油脂会导致肥胖、尽可能少吃 | |
| D. | 花生油、菜籽油、豆油等属植物油,可以食用;汽油、煤油、柴油属矿物油,绝对不能食用 |
10.某兴趣小组同学对实验室制取氧气的速率快慢进行如下探究实验.
(1)甲同学设计了以下对比试验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合,加热;
Ⅱ.将xg KClO3与1.0g CuO均匀混合,加热.
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的符号表达式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.Ⅱ中x的值为3.0.
甲同学实验的目的是比较不同物质的催化效果.
(2)乙同学探究了影响双氧水分解速率的某种因素,实验数据记录如表:
乙同学得到的实验结论是:在相同条件下,反应物的浓度越高,生成氧气速率越快.
(3)该兴趣小组继续探究二氧化锰用量对反应速率影响.他们做了这样一组实验:每次用30mL10%过氧化氢溶液,采用不同量二氧化锰粉末做实验,测定各收集到500mL氧气的所用时间,结果如下:(其他实验条件均相同)
请分析表中数据,得出结论:在一定范围内,加入的催化剂的量越多,反应速率也就越快.
(4)除上述影响因素外,还可能有哪些因素会影响双氧水分解速率,你的猜想是温度.
(5)拓展:催化剂在工业上应用较多.工业上用氢气和氮气在高温及催化剂的条件下合成氨气(NH3).请仔细观察如图,写出符合二者在催化剂表面反应,合成氨气的过程(将下面五张图按反应过程的先后顺序用序号排列)⑤④①②③.

(1)甲同学设计了以下对比试验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合,加热;
Ⅱ.将xg KClO3与1.0g CuO均匀混合,加热.
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的符号表达式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.Ⅱ中x的值为3.0.
甲同学实验的目的是比较不同物质的催化效果.
(2)乙同学探究了影响双氧水分解速率的某种因素,实验数据记录如表:
| 双氧水质量 | 双氧水浓度 | MnO2质量 | 相同时间内产生O2体积 | |
| I | 50.0g | 1% | 0.1g | 9mL |
| II | 50.0g | 2% | 0.1g | 16mL |
| III | 50.0g | 4% | 0.1g | 31mL |
(3)该兴趣小组继续探究二氧化锰用量对反应速率影响.他们做了这样一组实验:每次用30mL10%过氧化氢溶液,采用不同量二氧化锰粉末做实验,测定各收集到500mL氧气的所用时间,结果如下:(其他实验条件均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 二氧化锰用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 时间(秒) | 22 | 13 | 12 | 10 | 9 | 8 | 5 | 3 | 3 | 3 |
(4)除上述影响因素外,还可能有哪些因素会影响双氧水分解速率,你的猜想是温度.
(5)拓展:催化剂在工业上应用较多.工业上用氢气和氮气在高温及催化剂的条件下合成氨气(NH3).请仔细观察如图,写出符合二者在催化剂表面反应,合成氨气的过程(将下面五张图按反应过程的先后顺序用序号排列)⑤④①②③.

7.下列变化不属于物理变化的是( )
| A. | 将金刚石加工成钻石 | B. | 用活性炭除去冰箱中的异味 | ||
| C. | 将CO2制成干冰 | D. | 将CO2通入紫色石蕊溶液中 |
14.“康师傅方便面”是很多人喜爱的方便食品,其主要配料有:面饼、小麦粉、精炼棕榈油(含维生素E)、淀粉、食盐等,下列说法正确的是( )
| A. | 方便面中含有丰富的蛋白质,蛋白质仅由甘氨酸构成 | |
| B. | 方便面中含有大量淀粉,淀粉在人体内最终变成葡萄糖 | |
| C. | 方便面中含有人体所需的各种维生素 | |
| D. | 动物油和植物油合称为油脂 |
11.下列说法不正确的是( )
| A. | 当条件不变时,溶液放置时间稍长,溶质不会分离出来 | |
| B. | 溶液里各部分的性质是相同的 | |
| C. | 一种或一种以上的物质分散到另一种物质里形成的均一稳定的混合物叫溶液 | |
| D. | 凡是均匀、澄清、透明、稳定的液体就是溶液 |
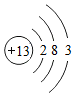 ;B离子
;B离子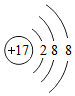 .
.