题目内容
【题目】按要求用元素符号或化学式完成下列填空
(1)3个硫原子_______________;
(2)氢氧根离子__________________;
(3)保持水的化学性质的微粒______________;
(4)碳酸氢铵的阳离子是_________________;
(5)氧化钙中钙元素的化合价为+2价______________。
【答案】3S OH- H2O NH4+ ![]()
【解析】
(1)元素符号前面数字表示原子个数,故3个硫原子可以表示为3S;
(2)氢氧根离子带一个单位的负电荷,符号为:OH-;
(3)由分子构成的物质,分子是保持物质化学性质的最小粒子,故保持水的化学性质的最小粒子为:H2O;
(4)碳酸氢铵是由阳离子铵根离子和阴离子碳酸氢根离子构成的,铵根离子带一个单位的正电荷,符号为:NH4+;
(5)化合价标在元素符号的正上方,氧化钙中钙元素的化合价为+2价,表示为:![]() 。
。

 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案【题目】为确定15.8g高锰酸钾完全分解能产生氧气的质量,小柯与小妍两位同学采用方法如下。根据他们测试方法,回答及计算:
小柯:实验测定法 | 小妍:计算法 |
在老师指导下,将15.8g高锰酸钾充分加热,得到氧气1120mL | 解:高锰酸钾中氧元素的质量分数: |
(1)大家经过讨论,认为小妍采用该方法计算氧气质量错误。理由是_______。
A 高锰酸钾中含氧元素
B 锰酸钾和二氧化锰中含氧元素
C 氧气中含氧元素
(2)已知:在小柯的实验条件下,氧气的密度为1.429g/L,小柯得到的氧气的质量_____(结果保留一位小数)。
(3)15.8g高锰酸钾完全分解产生的氧气的质量为__________(要求有解题过程)。
【题目】化学实验技能是学习化学和进行探究活动的基础和保证。以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究:
(提出问题)化学反应前后各物质的质量总和是否相等?
(猜想与假设)猜想1:不相等;猜想2:_____。
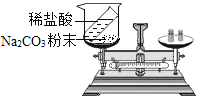
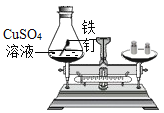
(实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 | 乙组 | |
实验方案(反应后略) |
|
|
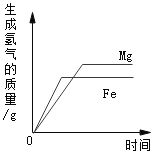
实验现象 | 有气泡产生,天平指针向右偏转 | 铁钉表面有红色物质析出,溶液由蓝色变为浅绿色,天平指针没有偏转 |
结论 | 猜想1正确 | 猜想2正确,反应的化学方程式:_____ |
(反思与评价)究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体逸出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在_____中进行。
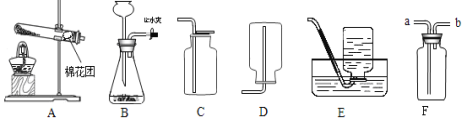
(优化装置)同学们对甲组左盘中的反应装置进行了如下三种改进,查阅资料后发现最佳装置是B,则猜想B中氢氧化钠具有的化学性质是_____。
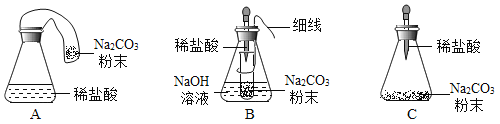
(得出结论)同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确。
【题目】要使世界更美好,必须学好好学。
Ⅰ.化学使生活更健康。
(1)自来水往往通过沉淀、_____、吸附、消毒杀菌等方法净化获得。
(2)为了预防碘缺乏症的发生,我国提倡食用加碘食盐,其中的“碘”是指_____。
A单质 B分子 C原子 D元素
(3)柚子皮可以吸附室内异味,写出一种具有同样性质的化学物质的名称_____。
Ⅱ.化学使能源更环保。
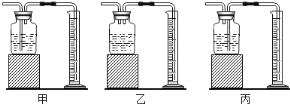
(1)绿色能源氢气可由如图电解水实验装置得到。该反应的化学方程式是_____,基本反应类型_____。通电后观察到的现象_____;a中气体的检验方法是_____;保持氢气化学性质的最小微粒是_____(写名称);
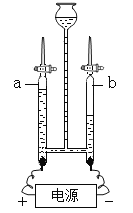
常温常压下,氢气和氧气的密度分别为1、2,则生成氢气和氧气的物质的量之比为_____(列出1、2的关系式)。
(2)当前,世界已经迈向了“低碳”时代,公交系统推广使用节能减排的双燃料公交车这种公交车以天然气为主要燃料。
a.下图为天然气的主要成分甲烷完全燃烧的化学反应的微观示意图。
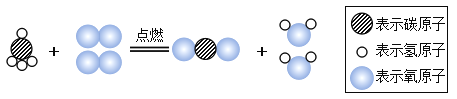
请根据示意图回答下列问题:从微粒观点分析,上述反应前后_____一定不变。反应的化学方程式是_____。
b.甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:
物质 | 甲烷 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 3.2 | 11.2 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
则a的值为_____;根据表格中数据,请完成相关的化学方程式:CH4+O2=_____。
Ⅲ.化学使食物更美味。
(1)七宝方糕,香气扑鼻。从分子角度解释“香气扑鼻”的原因是_____。
(2)七宝羊肉,香嫩入味。调味用的料酒主要成分是乙醇(C2H5OH),它一个分子中共含_____个原子,其中氢、氧元素质量比为_____;0.1mol乙醇为_____g,其中约含有分子_____个(用科学记数法表示)。