题目内容
【题目】为了分析生铁中铁的含量,某学习小组进行了实验研究.取4g生铁与10%的盐酸反应,并绘制了加入盐酸质与放出气体质的关系图(见下图).计算:
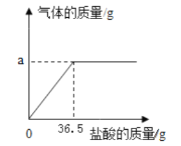
(说明:生铁中杂质不溶于水,不与盐酸、硫酸铜溶液反应.)
(1)放出气体的质量为多少?_____。
(2)生铁中铁的质量分数为多少?________。
(3)将完全反应后的溶液过滤,所得溶液中溶质的质量分数为多少? (最后计算结果保留两位小数)_______。
【答案】0.1g 70% 16%
【解析】
铁和稀盐酸反应生成氯化亚铁和氢气。
(1)设放出氢气的质量为x
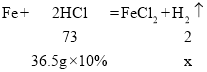
![]()
![]()
故放出气体的质量为0.1g。
(2)设生铁中铁的质量为y
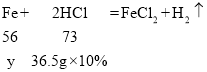
![]()
![]()
故生铁中铁的质量分数为![]()
(3)设生成FeCl2的质量为z
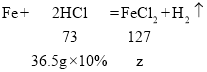
![]()
![]()
故所得溶液中溶质的质量分数为![]()

练习册系列答案
相关题目