题目内容
13.过氧化钠(Na2O2)为淡黄色固体,可作为潜水艇或呼吸面具的供养剂,人呼出气体主要成分有氮气、二氧化碳、水蒸气和氧气,Na2O2能分别与CO2、H2O反应,化学方程式为:2Na2O2+2CO2═2Na2CO3+O2↑;2Na2O2+2H2O═4NaOH+O2↑.某化学兴趣小组的同学开展了以下探究活动.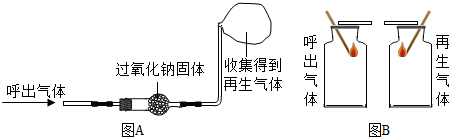
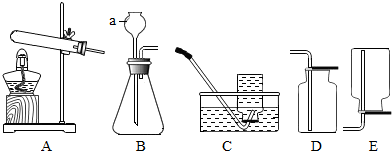
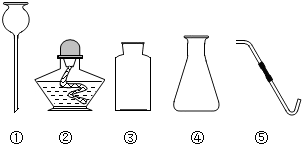
【实验探究一】将呼出气体通过如图A中的装置,收集得到一瓶再生气体.在收集一瓶呼出的气体.将两支燃着的同种木条分别同时伸入呼出气体和再生气体中,如图B,比较分析呼出气体和再生气体中氧气含量的多少.
【分析讨论】图B的实验是通过比较木条燃烧的剧烈程度来比较两种气体中氧气含量的多少.请说明呼吸面具或潜水艇用过氧化钠作为供氧剂的最大优点是将呼吸产生的二氧化碳处理掉.
实验探究一结束后,同学们将图A装置中的残留固体溶于水,得到了一杯无色溶液,他们对溶液的溶质成分进行探究:
【提出猜想】猜想Ⅰ:溶液是NaOH; 猜想Ⅱ:溶质是Na2CO3; 猜想Ⅲ:溶质是NaOH和Na2CO3
【实验探究二】取上述溶液少许于试管中,滴加澄清石灰水,若观察到有白色沉淀产生的现象,证明猜想Ⅰ不成立.
同学们经过实验探究证明猜想Ⅲ成立,请你写出证明猜想Ⅲ成立的实验步骤和现象.
| 实验步骤 | 实验现象 | 实验结论 |
| 1.取少量溶液于试管中; 2.加入 过量的氯化钙溶液; 3.过滤; 4.向滤液中滴加 酚酞试液. | 2. 产生白色沉淀; 4. 溶液变红. | 第2步反应的化学方程式是: Na2CO3+CaCl=CaCO3↓+2NaCl. 猜想Ⅲ成立. |
| 实验方案 | 反应的化学方程式 |
| 加入适量的氢氧化钙溶液,过滤 | Ca(OH)2+Na2CO3═CaCO3↓+2NaOH |
分析 【分析讨论】图B的实验是将燃着的木条分别伸入呼出气体和再生气体中,通过比较木条燃烧的剧烈程度来比较两种气体中氧气含量的多少;过氧化钠能与二氧化碳反应生成氧气;
【提出猜想】根据题中信息可知人呼出气体中有二氧化碳、水蒸气,过氧化钠和二氧化碳反应生成碳酸钠,和水反应生成氢氧化钠分析;
【实验探究二】根据氢氧化钠和碳酸钠的化学性质进行分析.
【实验探究三】根据提纯氢氧化钠需要除去碳酸钠解答.
解答 解:【分析讨论】图B的实验是将燃着的木条分别伸入呼出气体和再生气体中,通过比较木条燃烧的剧烈程度来比较两种气体中氧气含量的多少;用过氧化钠作为供氧剂的最大优点是呼吸产生的二氧化碳作为反应物,能废物再利用;
故填:木条燃烧的剧烈程度;将呼吸产生的二氧化碳处理掉;
【提出猜想】人呼出气体中有二氧化碳、水蒸气,而过氧化钠和二氧化碳反应生成碳酸钠,和水反应生成氢氧化钠,因此图A装置中的残留固体溶于水,可能形成的是碳酸钠溶液、可能是氢氧化钠溶液、也可能是两着的混合溶液;
故填:Na2CO3;
【实验探究二】碳酸钠和氢氧化钙反应生成碳酸钙沉淀,因此取上述溶液少许于试管中,滴加澄清石灰水,产生石灰水变浑浊,说明溶液中含有碳酸钠,可证明猜想Ⅰ不成立;
故填:白色沉淀;
氯化钙溶液显中性,氯化钙可与碳酸钠反应产生白色沉淀,因此取无色溶液少许于试管中,向其中加入过量(目的是将碳酸钠完全反应掉)的氯化钙溶液,有白色沉淀产生,说明有碳酸钠,过滤,再向滤液中加入无色酚酞试液,溶液变红,说明有氢氧化钠,证明猜想Ⅲ成立;
故填:
| 实验步骤 | 实验现象 | 实验结论 |
| 1.取少量溶液于试管中; 2.加入 过量的氯化钙溶液; 3.过滤; 4.向滤液中滴加 酚酞试液. | 2. 产生白色沉淀; 4. 溶液变红. | 第2步反应的化学方程式是: Na2CO3+CaCl=CaCO3↓+2NaCl. 猜想Ⅲ成立. |
| 实验方案 | 反应的化学方程式 |
| 加入适量的氢氧化钙溶液,过滤 | Ca(OH)2+Na2CO3═CaCO3↓+2NaOH |
点评 该考点的命题方向主要是以实验探究题的形式,给出有关的信息提示和相关数据,让学生通过实验探究,分析推断出该物质的组成成分;中考的重点是考查学生通过实验的方法来研究物质的组成成分以及含量能力.

 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案| A. | 氢气:产生白烟 | B. | 铁丝:产生白色固体 | ||
| C. | 红磷:生成五氧化二磷 | D. | 硫粉:明亮的蓝紫色火焰 |
| A. | 二氧化硫(SO2) | B. | 二氧化碳(CO2) | C. | 二氧化氮(NO2) | D. | 浮颗粒物(PM2.5) |
| A. | Ag | B. | Pb(铅) | C. | Cu | D. | Zn |
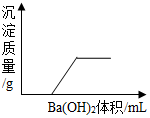 有一溶液是由盐酸、硫酸、硫酸铁、氯化铁、稀硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是( )
有一溶液是由盐酸、硫酸、硫酸铁、氯化铁、稀硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是( )| A. | 硝酸、硝酸铁 | B. | 硫酸、氯化铁 | C. | 盐酸、氯化铁 | D. | 盐酸、硫酸铁 |
【提出问题】白色粉末成分的猜想和成因分析.
【作出猜想】猜想Ⅰ:可能是CaCO3;原因是石灰水与空气中的CO2反应.
猜想Ⅱ:可能是Ca(OH)2 ;原因是溶剂蒸发,石灰水中的溶质结晶析出.
猜想Ⅲ:还可能是Ca(OH)2和CaCO3;原因是石灰水会与空气中的CO2反应,且溶剂蒸发时,石灰水中的溶质会结晶析出.
【实验探究】甲同学取白色粉末于试管中,加少量的水振荡,发现试管底部有白色固体.于是他得出白色固体粉末是CaCO3的结论.乙同学认为甲同学的结论不严密,理由是Ca(OH)2微溶于水.
为了得出较严密的结论,他们进行了如表所示实验,请完成实验报告:
| 实验步骤 | 实验现象 | 实验结论 |
| ?取上述试管中的上层清液,滴加1─2滴无色酚酞试液 | 溶液呈红色 | 白色粉末中含有Ca(OH)2 |
| ?往上述试管残留的白色固体中滴加稀盐酸 | 有气泡产生 | 白色粉末中含CaCO3 |
【拓展反思】通过上述实验的探究,同学们向实验员提出了保存易变质溶液的下列建议,合理的是ab.
a、密封保存 b、使用前临时配制 c、禁止使用该试剂.