题目内容
18.NO是大气污染物之一,但少量NO在人体内具有扩张血管、增强记忆的功能.NO密度比空气略大,难溶于水,通常条件下极易与氧气反应.实验室收集NO的装置是( )| A. |  | B. |  | C. |  | D. | 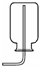 |
分析 收集气体有两种方法:排水法和排空气法,排水法适合于难溶于水且不和水反应的气体;排空气法有向上排空气法和向下排空气法两种,向上排空气法适合于密度比空气大而且不与空气成分发生反应的气体,向下排空气法适合于密度比空气小而且不与空气成分发生反应的气体.
解答 解:NO难溶于水,可用排水法收集;密度比空气的略大且极易和空气中的氧气反应,故不能用排空气法收集;
故选:C.
点评 排水法收集的气体较为纯净,是较为理想的收集方法.(一般有毒气体不适合用排空气的方法).

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
13.过氧化钠(Na2O2)为淡黄色固体,可作为潜水艇或呼吸面具的供养剂,人呼出气体主要成分有氮气、二氧化碳、水蒸气和氧气,Na2O2能分别与CO2、H2O反应,化学方程式为:2Na2O2+2CO2═2Na2CO3+O2↑;2Na2O2+2H2O═4NaOH+O2↑.某化学兴趣小组的同学开展了以下探究活动.
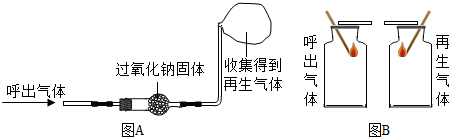
【实验探究一】将呼出气体通过如图A中的装置,收集得到一瓶再生气体.在收集一瓶呼出的气体.将两支燃着的同种木条分别同时伸入呼出气体和再生气体中,如图B,比较分析呼出气体和再生气体中氧气含量的多少.
【分析讨论】图B的实验是通过比较木条燃烧的剧烈程度来比较两种气体中氧气含量的多少.请说明呼吸面具或潜水艇用过氧化钠作为供氧剂的最大优点是将呼吸产生的二氧化碳处理掉.
实验探究一结束后,同学们将图A装置中的残留固体溶于水,得到了一杯无色溶液,他们对溶液的溶质成分进行探究:
【提出猜想】猜想Ⅰ:溶液是NaOH; 猜想Ⅱ:溶质是Na2CO3; 猜想Ⅲ:溶质是NaOH和Na2CO3
【实验探究二】取上述溶液少许于试管中,滴加澄清石灰水,若观察到有白色沉淀产生的现象,证明猜想Ⅰ不成立.
同学们经过实验探究证明猜想Ⅲ成立,请你写出证明猜想Ⅲ成立的实验步骤和现象.
【实验探究三】实验证明,“猜想Ⅲ”成立,请你设计一个提纯氢氧化钠的实验方案,以得到纯净的氢氧化钠溶液.

【实验探究一】将呼出气体通过如图A中的装置,收集得到一瓶再生气体.在收集一瓶呼出的气体.将两支燃着的同种木条分别同时伸入呼出气体和再生气体中,如图B,比较分析呼出气体和再生气体中氧气含量的多少.
【分析讨论】图B的实验是通过比较木条燃烧的剧烈程度来比较两种气体中氧气含量的多少.请说明呼吸面具或潜水艇用过氧化钠作为供氧剂的最大优点是将呼吸产生的二氧化碳处理掉.
实验探究一结束后,同学们将图A装置中的残留固体溶于水,得到了一杯无色溶液,他们对溶液的溶质成分进行探究:
【提出猜想】猜想Ⅰ:溶液是NaOH; 猜想Ⅱ:溶质是Na2CO3; 猜想Ⅲ:溶质是NaOH和Na2CO3
【实验探究二】取上述溶液少许于试管中,滴加澄清石灰水,若观察到有白色沉淀产生的现象,证明猜想Ⅰ不成立.
同学们经过实验探究证明猜想Ⅲ成立,请你写出证明猜想Ⅲ成立的实验步骤和现象.
| 实验步骤 | 实验现象 | 实验结论 |
| 1.取少量溶液于试管中; 2.加入 过量的氯化钙溶液; 3.过滤; 4.向滤液中滴加 酚酞试液. | 2. 产生白色沉淀; 4. 溶液变红. | 第2步反应的化学方程式是: Na2CO3+CaCl=CaCO3↓+2NaCl. 猜想Ⅲ成立. |
| 实验方案 | 反应的化学方程式 |
| 加入适量的氢氧化钙溶液,过滤 | Ca(OH)2+Na2CO3═CaCO3↓+2NaOH |
3.产生下列现象,只与空气中的水蒸气有关的是( )
| A. | 固体烧碱要密封存放 | |
| B. | 浓硫酸露置于空气中会增重、变稀 | |
| C. | 浓盐酸露置于空气中会变轻、变稀 | |
| D. | 铜制品长期放在空气中会产生“铜锈”[又称“铜绿”,化学式为Cu2(OH)2CO3] |
 如图是实验室常用来制取气体的装置,根据所学的知识回答以下问题:
如图是实验室常用来制取气体的装置,根据所学的知识回答以下问题:
 小意对自己使用的一节废旧干电池进行了系列探究;
小意对自己使用的一节废旧干电池进行了系列探究;