题目内容
8.被称为“绿色氧化剂”的过氧化氢(H2O2),俗称双氧水,是一种无色液体,常用作氧化剂、消毒杀菌剂和漂白剂等.在较低温度下和少量催化剂(如MnO2)条件下,它能迅速分解,生成氧气和水.请回答下列问题: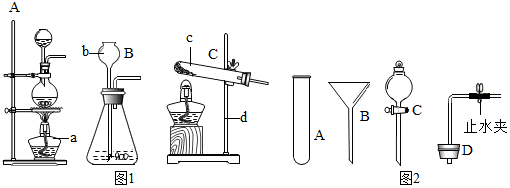
(1)写出图1中标号仪器的名称:b长颈漏斗 c试管
(2)若实验室用过氧化氢代替氯酸钾制取氧气,可采用哪种发生装置?B (填序号),
主要理由是反应物是固体和液体,不需要加热.
(3)当过氧化氢接触二氧化锰后,反应便立即开始并不能人为控制其速度.如果稍改变你所选择的装置,便可控制其反应的速度.请从图2的仪器中选择一种仪器更换你选择的装置中的一种仪器,以达到控制反应速度的目的.
你选择的仪器是C(填序号),它更换原装置中的b.控制反应速度的原理是:分液漏斗能够控制液体药品的流量,从而可知反应速率.
(3)天然气、沼气的主要成分是甲烷(CH4),它是无色无味的气体,密度比空气小,极难溶于水,能燃烧.实验室用无水醋酸钠和碱石灰固体混合物加热制取甲烷气体.若用此法制取甲烷气体,其气体发生装置选择C (从图1 A、B、C中选择) 可采用排水法或向下排空气法收集.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(3)分液漏斗能够控制液体药品的流量,从而可以控制反应速率;
(3)根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置.
解答 解:(1)b是长颈漏斗,c是试管.
故填:长颈漏斗;试管.
(2)实验室用过氧化氢制取氧气不需要加热,应该用B装置作为发生装置,理由是:反应物是固体和液体,不需要加热.
故填:B;反应物是固体和液体,不需要加热.
(3)选择的仪器是C,它更换原装置中的b,控制反应速度的原理是:分液漏斗能够控制液体药品的流量,从而可知反应速率.
故填:C;b;分液漏斗能够控制液体药品的流量,从而可知反应速率.
(3)实验室用无水醋酸钠和碱石灰固体混合物加热制取甲烷气体时,其气体发生装置选择C;
甲烷不溶于水,可以用排水法收集,密度比空气小,可以用向下排空气法收集.
故填:C;排水法;向下排空气法.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
18.下列说法正确的是( )
| A. | “绿色食品”都是绿色的植物 | |
| B. | 植物的光合作用有益于生态平衡 | |
| C. | 吸烟会危害人体健康,但不会污染环境 | |
| D. | 发电厂热水直接排入江河,有利于鱼类生存 |
16.加热24.5克氯酸钾和含少量二氧化锰的混合物,当质量减少了9.6克时,停止加热、则反应剩余物中含有的是( )
| A. | KClO3、KCl | B. | KCl、KClO3、MnO2 | C. | KCl | D. | KCl、MnO2 |
3.下列物质中属于纯净物的是( )
| A. | 洁净的空气 | B. | 酸奶 | C. | 糖水 | D. | 蒸馏水 |
13.自来水是我国目前主要的生活饮用水,下表是我国颁布的生活饮用水水质标准的部分内容:
(1)感官指标表现的是自来水的物理(填“物理”或“化学”)性质.
(2)自来水中的游离氯有少量可转变为氯离子,氯离子的符号是Cl-.
(3)实验室用自来水制取蒸馏水的方法是D(填序号).
A.吸附 B.沉淀 C.过滤 D.蒸馏.
| 项目 | 标准 |
| 感官指标 | 无异味、异臭等 |
| 化学指标 | pH 6.5-8.5,铜<1.0mg•L-1,铁<0.3mg•L-1, 氟化物<1.0mg•L-1,游离氯≥0.3mg•L-1等 |
(2)自来水中的游离氯有少量可转变为氯离子,氯离子的符号是Cl-.
(3)实验室用自来水制取蒸馏水的方法是D(填序号).
A.吸附 B.沉淀 C.过滤 D.蒸馏.
10.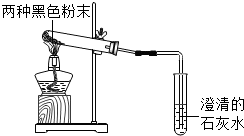 同学们在实验室发现了两瓶失去标签的黑色粉末药品,并确定了这两瓶黑色粉末是木炭、铁粉、氧化铜、高锰酸钾中的两种.他们由此进行了实验探究:
同学们在实验室发现了两瓶失去标签的黑色粉末药品,并确定了这两瓶黑色粉末是木炭、铁粉、氧化铜、高锰酸钾中的两种.他们由此进行了实验探究:
【讨论分析】小聪同学认为一定不是高锰酸钾,原因是高锰酸钾是暗紫色不是黑色的;
【实验探究一】
结论:根据上述分析和实验可得出另一黑色粉末是木炭粉;
【实验探究二】
进一步确认固体成分
将两种黑色粉末混合按如图装置进行实验,预想的实验现象为:黑色粉末逐渐变红色,澄清石灰水变浑浊.写出两种黑色粉末发生反应的化学方程式2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
 同学们在实验室发现了两瓶失去标签的黑色粉末药品,并确定了这两瓶黑色粉末是木炭、铁粉、氧化铜、高锰酸钾中的两种.他们由此进行了实验探究:
同学们在实验室发现了两瓶失去标签的黑色粉末药品,并确定了这两瓶黑色粉末是木炭、铁粉、氧化铜、高锰酸钾中的两种.他们由此进行了实验探究:【讨论分析】小聪同学认为一定不是高锰酸钾,原因是高锰酸钾是暗紫色不是黑色的;
【实验探究一】
| 实验操作 | 实验现象 | 实验结论 |
| ①取一种黑色粉末少许,加入到稀硫酸中 | 黑色粉末溶解,溶液颜色变蓝色 | 此粉末是氧化铜 |
| ②取另一种黑色粉末少许,加入到稀硫酸中 | 黑色粉末不溶解,没看到气体产生 | 此粉末一定不是铁粉 |
【实验探究二】
进一步确认固体成分
将两种黑色粉末混合按如图装置进行实验,预想的实验现象为:黑色粉末逐渐变红色,澄清石灰水变浑浊.写出两种黑色粉末发生反应的化学方程式2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.