题目内容
13. 现有Ca(OH)2、CaCO3和一些杂质(不与稀盐酸反应)组成的混合物共15g,取某浓度的稀盐酸,逐滴滴加到混合物中,充分反应,测得稀盐酸的质量与反应生成气体的质量,关系如图所示:
现有Ca(OH)2、CaCO3和一些杂质(不与稀盐酸反应)组成的混合物共15g,取某浓度的稀盐酸,逐滴滴加到混合物中,充分反应,测得稀盐酸的质量与反应生成气体的质量,关系如图所示:(1)生成CO2的质量是2.2g;
(2)计算混合物中CaCO3的质量分数.(写出计算过程,结果精确到0.1%)
(3)所取稀盐酸的浓度是18.25%,欲配制100g该浓度的稀盐酸,需要溶质质量分数为36.5%的盐酸50g.
分析 (1)根据图可知反应生成了2.2g的二氧化碳,这来自于碳酸钙和盐酸的反应,而加入盐酸到40g时,是盐酸和氢氧化钙反应,所以没有气体产生,当加入盐酸到60g时,碳酸钙也恰好完全反应,所以继续加入盐酸时,盐酸过量.
(2)碳酸钙的质量分数求算要先根据二氧化碳求出碳酸钙,然后再计算碳酸钙的质量分数.
(3)根据二氧化碳求出氯化氢的质量,然后再计算溶质的质量分数,再根据混合前后溶质的质量不变分析.
解答 解:(1)根据图可知反应生成二氧化碳的质量为2.2g;故填:2.2;
(2)设样品中碳酸钙的质量为x.需要氯化氢的质量为y.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 2.2g
$\frac{100}{x}=\frac{73}{y}=\frac{44}{2.2g}$
x=5g,y=3.65g
则样品中碳酸钙的质量分数为$\frac{5g}{15g}$×100%≈33.3%;
答:样品中碳酸钙的质量分数为33.3%;
(3)所取稀盐酸的浓度是$\frac{3.65g}{60g-40g}×$100%=18.25%,
设需要溶质质量分数为36.5%的盐酸z
36.5%×z=100g×18.25%
z=50g
答:所取稀盐酸的浓度是18.25%,
需要溶质质量分数为36.5%的盐酸50g.
点评 图表型计算题,首先要根据图表提炼有效的数据进行方程式的计算,也就是确定数字的有效性.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目
1.磷肥促使作物根系发达,增强抗寒抗旱能力.下列属于磷肥的是( )
| A. | KCl | B. | Na2SO4 | C. | NH4HCO3 | D. | Ca(H2PO4)2 |
4.下列操作中,从物质变化的角度分析,主要体现化学变化的是( )
| A. | 木材加工成古典家具 | B. | 新鲜鸭梨榨汁 | ||
| C. | 鸭梨汁酿造食醋 | D. | 不锈钢餐具抛光 |
8. 2016年12月,华为公司宣布即将推出高温长寿命石墨烯基锂离子电池.石墨烯是由碳原子构成的六边形单元向外延展而成的蜂窝状结构(如图所示).下列说法正确的是( )
2016年12月,华为公司宣布即将推出高温长寿命石墨烯基锂离子电池.石墨烯是由碳原子构成的六边形单元向外延展而成的蜂窝状结构(如图所示).下列说法正确的是( )
 2016年12月,华为公司宣布即将推出高温长寿命石墨烯基锂离子电池.石墨烯是由碳原子构成的六边形单元向外延展而成的蜂窝状结构(如图所示).下列说法正确的是( )
2016年12月,华为公司宣布即将推出高温长寿命石墨烯基锂离子电池.石墨烯是由碳原子构成的六边形单元向外延展而成的蜂窝状结构(如图所示).下列说法正确的是( )| A. | 石墨烯是人工合成的化合物 | |
| B. | 石墨烯与石墨分别在氧气中完全燃烧的产物不同 | |
| C. | 石墨烯的碳原子排列方式与金刚石的相同 | |
| D. | 石墨烯转变成金刚石是一种化学变化 |
3.下列净化水的方法,净化程度最高的是( )
| A. | 沉降 | B. | 过滤 | C. | 蒸馏 | D. | 吸附 |
 水是人类宝贵的自然资源.
水是人类宝贵的自然资源.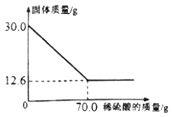 菱铁矿(主要成分是FeCO3)是炼铁的原料,现取30.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图所示.
菱铁矿(主要成分是FeCO3)是炼铁的原料,现取30.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图所示.