题目内容
19.质监部门常采用“盖尔达法”鉴定奶粉的优劣.其原理是:把奶粉中的氮元素转化为NH3,再用一定量的稀硫酸来吸收[2NH3+H2SO4=(NH4)2SO4],从而计算出奶粉中氮元素的质量数,确定奶粉是否合格.(奶粉中氮元素的质量分数达到16%为合格)现取某奶粉样品20g,将其中的氮元素转化为NH3,用100g溶质质量分数为9.8%的稀硫酸恰好完全反应.
(1)计算产生NH3的质量.
(2)通过计算判断该奶粉是否合格.
分析 (1)根据氨气与硫酸反应的化学方程式,由吸收氨气消耗硫酸的质量计算氨气的质量;
(2)根据检测蛋白质的方法可知,所吸收氨气中的N元素质量即所取20g奶粉样品中N元素的质量分数,利用所取奶粉样品中N元素的质量分数与国家标准对比,判断所取奶粉是否合格
解答 解:(1)设生成氨气的质量为x
2NH3+H2SO4=(NH4)2SO4
34 98
X 100g×9.8%
$\frac{34}{x}=\frac{98}{100g×9.8%}$
X=3.4g
(2)奶粉中N元素的质量分数:$\frac{3.4g×\frac{14}{17}}{20g}$×100%=14%
小于16%,所以该奶粉不合格
答:(1)生成氨气的质量为3.4g
(2)不合格.
点评 此题考查根据化学方程式的计算,此题解答较困难,综合性强,另外使学生明确一定质量的化合物中某元素的质量=化合物的质量×化合物中该元素的质量分数.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
3. 氢气是很好的能源物质,但不便于储存和运输.氢化钙是一种储氢材料,其储存和释放氢气的过程如图所示:下列判断不正确的是( )
氢气是很好的能源物质,但不便于储存和运输.氢化钙是一种储氢材料,其储存和释放氢气的过程如图所示:下列判断不正确的是( )
 氢气是很好的能源物质,但不便于储存和运输.氢化钙是一种储氢材料,其储存和释放氢气的过程如图所示:下列判断不正确的是( )
氢气是很好的能源物质,但不便于储存和运输.氢化钙是一种储氢材料,其储存和释放氢气的过程如图所示:下列判断不正确的是( )| A. | 储氢过程发生化合反应 | B. | 释放氢的过程发生复分解反应 | ||
| C. | 氢气属于绿色能源 | D. | 保存氢化钙应注意防潮 |
10.KNO3、NaNO3等硝酸盐中氮元素的化合价为( )
| A. | -1 | B. | 0 | C. | +3 | D. | +5 |
14.适量摄入维生素能提高人体免疫力,下列食物中富含维生素的是( )
| A. |  米饭 | B. |  花生 | C. |  橙子 | D. |  豆腐 |
11.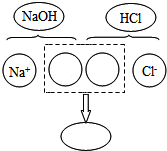 酸、碱、盐在生活中应用广泛.请根据图示回答相关问题:
酸、碱、盐在生活中应用广泛.请根据图示回答相关问题:
(1)从微观角度看物质的变化是化学的思维方式之一.如图表示生成氯化钠的化学反应,该反应的化学方程式是NaOH+HCl=NaCl+H2O,其微观实质是OH-与H+结合生成H2O分子.
(2)对比学习有利于发现事物的共性与个性.为探究酸的化学性质,某同学进行了如下实验.
请分析上述现象并回答:
清洗试管时,将C、F两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡并出现白色沉淀.废液缸里最终产生的白色沉淀中一定含有硫酸钡,该反应的化学方程式为Na2SO4+BaCl2=2NaCl+BaSO4↓,白色沉淀中可能还含有BaCO3(填化学式).
 酸、碱、盐在生活中应用广泛.请根据图示回答相关问题:
酸、碱、盐在生活中应用广泛.请根据图示回答相关问题:(1)从微观角度看物质的变化是化学的思维方式之一.如图表示生成氯化钠的化学反应,该反应的化学方程式是NaOH+HCl=NaCl+H2O,其微观实质是OH-与H+结合生成H2O分子.
(2)对比学习有利于发现事物的共性与个性.为探究酸的化学性质,某同学进行了如下实验.
| 实验内容 | 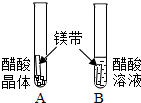 | 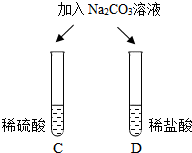 |  |
| 实验现象 | A试管内无明显现象,B试管中镁带表面观察到的现象是有气泡产生或冒气泡. | C、D两试管中均观察到有气泡产生. | E试管中观察到的现象是 产生白色沉淀; F试管中无明显现象. |
| 结论 | 酸的很多反应通常在水溶液中才能完成. | 酸具有相似的化学性质或酸能与碳酸盐反应生成CO2 | 不同的酸根会导致酸的“个性”有差异. |
清洗试管时,将C、F两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡并出现白色沉淀.废液缸里最终产生的白色沉淀中一定含有硫酸钡,该反应的化学方程式为Na2SO4+BaCl2=2NaCl+BaSO4↓,白色沉淀中可能还含有BaCO3(填化学式).
8.取镁、碳酸镁组成的固体混合物20.4g,放入325g稀硫酸中,恰好完全反应,得到5.4g气体和溶质质量分数为20%的溶液,则原固体混合物中镁元素的质量为( )
| A. | 4.8g | B. | 9.6g | C. | 13.6g | D. | 16.8g |
9.实验室配制100g 6%的氯化钠溶液,有关实验操作不正确的是( )
| A. | 用托盘天平称取6.0g氯化钠 | |
| B. | 用量筒量取94.0mL的水 | |
| C. | 将称取的氯化钠倒入量筒中溶解 | |
| D. | 将配制的溶液装入试剂瓶中,贴上标签 |
 如图为甲、乙、丙三种物质的溶解度曲线,据图回答:
如图为甲、乙、丙三种物质的溶解度曲线,据图回答: