题目内容
8.工业上生产印刷线路板及废液处理的过程如图所示.下列分析正确的是( )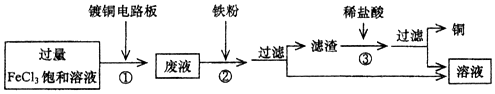
| A. | ①中参加反应的氯化铁和铜的质量之比为2:1 | |
| B. | 废液中含有一种溶质 | |
| C. | ②中铁粉过量 | |
| D. | ②中有化合反应发生 |
分析 根据金属的性质以及物质间反应的实验现象进行分析解答即可.
解答 解:A、铜和氯化铁反应生成氯化亚铁和氯化亚铜,该反应的化学方程式为:Cu+2FeCl3=CuCl2+2FeCl2,故氯化铁和铜的质量比为:64:(2×162.5)=64:325≠2:1,错误;
B、废液中含有氯化铜和氯化亚铁以及过量的氯化铁,溶质不是一种,错误;
C、②中加入铁粉过滤得到的滤渣中加入盐酸能得到氯化亚铁,故铁粉过量,正确;
D、②中有铁和氯化铁的反应,是化合反应,正确;
故选CD.
点评 本题考查的是金属的性质以及应用,完成此题,可以依据已有的金属的性质进行.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
18.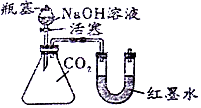 CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究
CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究
【查阅资料】①通常情况下,1体积水溶解1体积的CO2;
②在一定浓度的溶液中,有微溶物生成的复分解反应也能发生.
【实验探究】小红同学设计了如图所示的实验装置(锥形瓶内充满CO2),并进行实验
打开瓶塞和活塞,使NaOH溶液快速滴入锥形瓶中,立即关闭活塞(漏斗中仍有溶液剩余),观察到U型管右侧的红墨水液面降低(填“升高”、“降低”或“不移动”),小红根据现象判断CO2和NaOH发生了反应,理由是U型管内右侧液面下降,说明锥形瓶内的压强减小,从而说明氢氧化钠与二氧化碳发生了反应.
【反思与评价】小明认为小红的实验方案不严密,理由是二氧化碳溶于水也会使锥形瓶内的压强变小.
【拓展实验】兴趣小组的同学们为此又设计了如表所示的两种方法,进一步探究,请填写表格
【反思与评价2】同学们经过讨论,认为【拓展实验】的方法一(填“方法一”或“方法二”)依然不严密,理由是2NaOH+CaCl2═Ca(OH)2↓+2NaCl(用化学方程式表示).
 CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究
CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究【查阅资料】①通常情况下,1体积水溶解1体积的CO2;
②在一定浓度的溶液中,有微溶物生成的复分解反应也能发生.
【实验探究】小红同学设计了如图所示的实验装置(锥形瓶内充满CO2),并进行实验
打开瓶塞和活塞,使NaOH溶液快速滴入锥形瓶中,立即关闭活塞(漏斗中仍有溶液剩余),观察到U型管右侧的红墨水液面降低(填“升高”、“降低”或“不移动”),小红根据现象判断CO2和NaOH发生了反应,理由是U型管内右侧液面下降,说明锥形瓶内的压强减小,从而说明氢氧化钠与二氧化碳发生了反应.
【反思与评价】小明认为小红的实验方案不严密,理由是二氧化碳溶于水也会使锥形瓶内的压强变小.
【拓展实验】兴趣小组的同学们为此又设计了如表所示的两种方法,进一步探究,请填写表格
| 实验方法 | 操作过程 | 现象 | 实验结论 |
| 方法一 | 取小红实验后锥形瓶内的溶液适量,加入足量CaCl2溶液 | 产生白色沉淀 | CO2与NaOH发生了反应 |
| 方法二 | 取小红实验后锥形瓶内的溶液适量,加入足量稀盐酸; | 有气泡产生 |
19. 目前,一种人称“摇摇冰”的即冷即用饮料开始上市.所谓“摇摇冰”是指吸食前将饮料罐隔离层中的制冷物质和水混合摇动,能使罐中的饮料冷却.若该制冷物质可以在下列物质中选择,它应该是( )
目前,一种人称“摇摇冰”的即冷即用饮料开始上市.所谓“摇摇冰”是指吸食前将饮料罐隔离层中的制冷物质和水混合摇动,能使罐中的饮料冷却.若该制冷物质可以在下列物质中选择,它应该是( )
 目前,一种人称“摇摇冰”的即冷即用饮料开始上市.所谓“摇摇冰”是指吸食前将饮料罐隔离层中的制冷物质和水混合摇动,能使罐中的饮料冷却.若该制冷物质可以在下列物质中选择,它应该是( )
目前,一种人称“摇摇冰”的即冷即用饮料开始上市.所谓“摇摇冰”是指吸食前将饮料罐隔离层中的制冷物质和水混合摇动,能使罐中的饮料冷却.若该制冷物质可以在下列物质中选择,它应该是( )| A. | 食盐 | B. | 硝酸铵 | C. | 氢氧化钠 | D. | 酒精 |
3.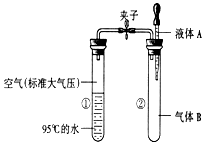 如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B的组合可能是下列的( )
如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B的组合可能是下列的( )
 如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B的组合可能是下列的( )
如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B的组合可能是下列的( )| A. | 氢氧化钙溶液、一氧化碳 | B. | 硝酸银、氯化氢 | ||
| C. | 酒精、氧气 | D. | 水、甲烷 |
13.缺乏维生素A(化学式为C20H30O),会引起夜盲证.下列说法正确的是( )
| A. | 维生素A的相对分子质量286g | |
| B. | 维生素A中碳、氢、氧元素的质量比为20:30:1 | |
| C. | 维生素A中碳元素的质量分数是83.9% | |
| D. | 维生素A是由20个碳原子、30个氢原子、1个氧原子构成的 |
20.某同学为探究镁、锌、铜、银的活动性顺序,设计如下实验流程,依据该流程设计,下面对物质①、②的选择合理的是( )
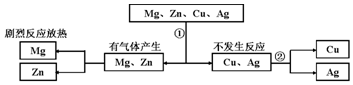

| A. | ①稀硫酸②硫酸汞 | B. | ①稀盐酸 ②硫酸锌 | ||
| C. | ①稀盐酸 ②硫酸亚铁 | D. | ①稀硫酸 ②氯化镁 |


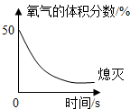 足量蜡烛(由碳、氢元素组成)在密闭集气瓶内(起始时常压)燃烧至熄灭,瓶内氧气体积分数随时间变化如图所示.下列说法正确的是( )
足量蜡烛(由碳、氢元素组成)在密闭集气瓶内(起始时常压)燃烧至熄灭,瓶内氧气体积分数随时间变化如图所示.下列说法正确的是( )