题目内容
19. 目前,一种人称“摇摇冰”的即冷即用饮料开始上市.所谓“摇摇冰”是指吸食前将饮料罐隔离层中的制冷物质和水混合摇动,能使罐中的饮料冷却.若该制冷物质可以在下列物质中选择,它应该是( )
目前,一种人称“摇摇冰”的即冷即用饮料开始上市.所谓“摇摇冰”是指吸食前将饮料罐隔离层中的制冷物质和水混合摇动,能使罐中的饮料冷却.若该制冷物质可以在下列物质中选择,它应该是( )| A. | 食盐 | B. | 硝酸铵 | C. | 氢氧化钠 | D. | 酒精 |
分析 由题意可知该物质与水混合会吸热使温度降低,才能达到制冷的效果.要从物质溶于水后热量变化来考虑.
解答 解:吸食前将饮料隔离层中的制冷物质和水混合摇动能使罐中饮料冷却,选择的物质溶于水应吸热,使溶液温度降低.
A、食盐溶于水温度几乎无变化,故选项错误.
B、硝酸铵固体溶于水吸热,温度降低,故选项正确.
C、氢氧化钠溶于水温度升高,故选项错误.
D、酒精溶于水温度几乎无变化,故选项错误.
故选:B.
点评 本题难度不大,掌握常见物质溶于水或与水反应的吸热与放热现象、温度变化情况是正确解答本题的关键.

练习册系列答案
相关题目
4.在中学所学的化学反应中,有很多反应没有明显现象.某探究小组想通过实验来证明CO2与NaOH溶液反应确实发生了,他们做了以下探究过程.
【查阅资料】通常状况下,1体积水能溶解1体积二氧化碳.
【设计实验】甲同学设计了三个实验进行验证,请你帮他完成下列实验报告.
密封线内不得答题
【反思交流】
(1)实验①由于甲同学选用的仪器不当,导致未能观察到明显现象,乙同学将甲同学的广口瓶替换成塑料瓶,看到了塑料瓶变瘪现象,证明CO2可以与NaOH溶液反应.丙同学认为乙同学的改进实验仍然存在缺陷,应增加一个对比实验,证明CO2确实可以与NaOH溶液发生反应,该对比实验所用的试剂是水和二氧化碳 .
(2)请判断③中V>200mL(填“>”、“<”或“=”),理由是如果没有NaOH溶液,V≤200mL时CO2能够完全溶于水也会产生同样现象.
【实验结论】通过实验探究,证明了氢氧化钠溶液可以与二氧化碳反应.
【查阅资料】通常状况下,1体积水能溶解1体积二氧化碳.
【设计实验】甲同学设计了三个实验进行验证,请你帮他完成下列实验报告.
| 实验操作 | 实验现象 | 实验结论及解释 | |
| ① |  | 氢氧化钠溶液可以与CO2反应, 反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O | |
| ② |  | 气球膨胀 | 氢氧化钠溶液可以与CO2反应. |
| ③ |  洗气瓶中的溶液为氢氧化钠溶液或澄清石灰水(均为200mL) | A,B均无明显变化 | 氢氧化钠溶液可以与CO2反应. B中盛放的溶液是澄清石灰水. |
【反思交流】
(1)实验①由于甲同学选用的仪器不当,导致未能观察到明显现象,乙同学将甲同学的广口瓶替换成塑料瓶,看到了塑料瓶变瘪现象,证明CO2可以与NaOH溶液反应.丙同学认为乙同学的改进实验仍然存在缺陷,应增加一个对比实验,证明CO2确实可以与NaOH溶液发生反应,该对比实验所用的试剂是水和二氧化碳 .
(2)请判断③中V>200mL(填“>”、“<”或“=”),理由是如果没有NaOH溶液,V≤200mL时CO2能够完全溶于水也会产生同样现象.
【实验结论】通过实验探究,证明了氢氧化钠溶液可以与二氧化碳反应.
11. 反应物的温度、浓度、固体反应物的颗粒大小等因素会影响化学反应速率.为研究实验室制取二氧化碳的适宜条件,进行如下四组实验:
反应物的温度、浓度、固体反应物的颗粒大小等因素会影响化学反应速率.为研究实验室制取二氧化碳的适宜条件,进行如下四组实验:
(1)大理石与盐酸反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)实验甲与丙对照(填编号),是为了研究固体反应物颗粒大小对反应速率的影响.
(3)上述实验中,另一个影响反应速率的因素是盐酸的质量分数.
(4)如表是小明同学按照乙组进行实验测定生成二氧化碳体积的实验数据.
请解释大理石与稀盐酸反应速率逐渐减慢的原因盐酸溶液的质量分数减少.
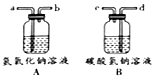
(5)除去二氧化碳气体中混有的氯化氢气体,选用图中的B(填字母,下同),将混合气体从d端通入.
(6)请完成探究温度对反应速率影响的数据
 反应物的温度、浓度、固体反应物的颗粒大小等因素会影响化学反应速率.为研究实验室制取二氧化碳的适宜条件,进行如下四组实验:
反应物的温度、浓度、固体反应物的颗粒大小等因素会影响化学反应速率.为研究实验室制取二氧化碳的适宜条件,进行如下四组实验:| 甲 | 乙 | 丙 | 丁 | |
| 大理石/(等量) | 块状 | 块状 | 粉末状 | 粉末状 |
| 盐酸/(质量分数) | 5% | 10% | 5% | 10% |
| 收集50mL二氧化碳所需时间/(秒) | 118 | 60 | 70 | 50 |
(2)实验甲与丙对照(填编号),是为了研究固体反应物颗粒大小对反应速率的影响.
(3)上述实验中,另一个影响反应速率的因素是盐酸的质量分数.
(4)如表是小明同学按照乙组进行实验测定生成二氧化碳体积的实验数据.
| 时段 | 第10秒 | 第20秒 | 第30秒 | 第40秒 | 第50秒 | 第60秒 |
| CO2体积 | 13 | 11 | 9 | 8 | 5 | 4 |
(5)除去二氧化碳气体中混有的氯化氢气体,选用图中的B(填字母,下同),将混合气体从d端通入.
(6)请完成探究温度对反应速率影响的数据
| 甲 | 乙 | |
| 大理石/(等量) | 块状 | 块状 |
| 盐酸/(质量分数) | 10% | 10% |
| 盐酸质量/(g) | 100 | 100 |
| 盐酸温度/℃ | 20 | 30 |
8.工业上生产印刷线路板及废液处理的过程如图所示.下列分析正确的是( )
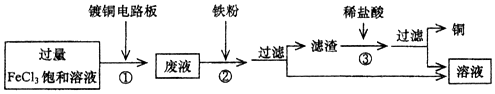

| A. | ①中参加反应的氯化铁和铜的质量之比为2:1 | |
| B. | 废液中含有一种溶质 | |
| C. | ②中铁粉过量 | |
| D. | ②中有化合反应发生 |
9.多数食品易吸收空气中的水分变潮,并与空气中的O2 反应腐败.生产上多在食品上放入一包CaO粉未,使食品保持干燥.现已研究成功在食品中放入一包铁粉(包裹在多孔泡沫中)铁粉吸收水分和氧气变成铁锈,从而保护食品.下列说法不正确的( )
| A. | 两干燥剂袋上都要有明显的“勿食”字样 | |
| B. | 生成铁锈的主要成分是氧化铁 | |
| C. | 铁粉干燥剂能与水和O2 发生化学反应 | |
| D. | CaO干燥剂保护食品的效果比铁粉干燥剂好 |



