题目内容
11.同学们在完成下列关于氧气的实验后,回答以下问题.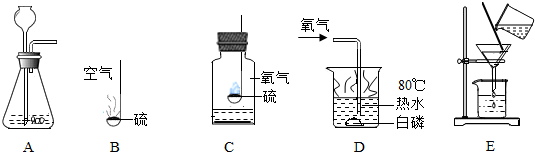
(1)实验室用装置A制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)图B、C表示完全相同的两份硫分别在空气和氧气中燃烧的实验,B中观察到的现象是发出淡蓝色火焰,放热,生成有刺激性气味的气体,对比B、C中的现象,你能得到的结论是氧气的浓度越大,燃烧现象越剧烈(合理均可).
(3)图D表示热水中的白磷在通入氧气后才开始燃烧,由此得出燃烧所需的条件之一是可燃物与氧气接触.
(4)氧气制取完毕后,实验室回收二氧化锰的操作方法是过滤、烘干;请指出图E中的错误(写出一条)漏斗下端未紧靠烧杯内壁(或烧杯口未紧贴玻璃棒、液面高于滤纸边缘).
分析 (1)装置A属于固液常温型,实验室利用过氧化氢溶液常温分解制取氧气可用此装置,据反应原理书写方程式;
(2)据硫在氧气和空气中燃烧的现象解答;
(3)热水中的白磷在通入氧气后才开始燃烧,由此得出燃烧所需的条件之一是可燃物要与氧气接触;
(4)二氧化锰不溶于水,所以回收二氧化锰可先过滤,然后再烘干;并据过滤操作的注意事项结合图示解答.
解答 解:(1)装置A属于固液常温型,实验室利用过氧化氢溶液常温分解制取氧气可用此装置,过氧化氢在二氧化锰的催化作用下生成水和氧气,反应方程式是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)硫在空气中燃烧发出淡蓝色火焰,放热,生成有刺激性气味的气体,在氧气中燃烧更旺,发出明亮的蓝紫色火焰,由此可见:氧气的浓度越大,燃烧现象越剧烈;
(3)热水中的白磷在通入氧气后才开始燃烧,由此得出燃烧所需的条件之一是可燃物要与氧气接触;
(4)二氧化锰不溶于水,所以回收二氧化锰可先过滤,然后再烘干;图示操作存在的错误有:漏斗下端未紧靠烧杯内壁、烧杯口未紧贴玻璃棒、液面高于滤纸边缘;
故答案为:(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)发出淡蓝色火焰,放热,生成有刺激性气味的气体;氧气的浓度越大,燃烧现象越剧烈(合理均可);
(3)可燃物与氧气接触;
(4)过滤、烘干;漏斗下端未紧靠烧杯内壁(或烧杯口未紧贴玻璃棒、液面高于滤纸边缘).
点评 了解燃烧的条件、过氧化氢制取氧气的反应原理、过滤操作等知识是解答问题的关键,难度不大,能较好考查学生分析、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.在元素周期表中,应用于计算机芯片的硅元素如图所示,下列硅的说法正确的是( )


| A. | 原子序数是14 | B. | “--”中硅元素符号是SI | ||
| C. | 相对原子质量是14 | D. | 质子数是28.05 |
2.某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多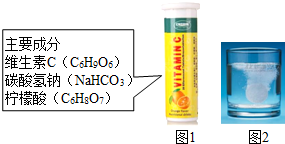 气泡产生(如图2).该小组同学进行如下探究.
气泡产生(如图2).该小组同学进行如下探究.
探究一:该气体的成分.
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、
N2.
小明说:不可能含有N2,因为维C泡腾片和水中无氮元素.
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,
H2易燃易爆,CO 有毒;
该小组同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
【得出结论】
(1)由实验①可知,该气体中肯定含有CO2.写出该反应的化学方程式CO2+Ca(OH)2=CaCO3↓+H2O.
(2)由实验②不能(填“能”或“不能”)确定该气体中不含氧气.
探究二:维C泡腾片溶液的酸碱性.向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显酸性.
 气泡产生(如图2).该小组同学进行如下探究.
气泡产生(如图2).该小组同学进行如下探究.探究一:该气体的成分.
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、
N2.
小明说:不可能含有N2,因为维C泡腾片和水中无氮元素.
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,
H2易燃易爆,CO 有毒;
该小组同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(1)由实验①可知,该气体中肯定含有CO2.写出该反应的化学方程式CO2+Ca(OH)2=CaCO3↓+H2O.
(2)由实验②不能(填“能”或“不能”)确定该气体中不含氧气.
探究二:维C泡腾片溶液的酸碱性.向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显酸性.
19.下列属于化学变化的是( )
| A. | 风力发电 | B. | 酒精挥发 | C. | 液氮汽化 | D. | 秸秆焚烧 |
6. 下列实验过程与如图相符的是( )
下列实验过程与如图相符的是( )
 下列实验过程与如图相符的是( )
下列实验过程与如图相符的是( )| A. | 加热氯酸钾 | |
| B. | 向稀硫酸中滴入氯化钡溶液 | |
| C. | 向氯化钠溶液中滴加硝酸钾溶液 | |
| D. | 向装有生锈铁钉的试管中倒入少量稀硫酸 |
16.下列关于能源说法中正确的是( )
| A. | 煤、石油、太阳能都是不可再生能源 | |
| B. | 风能、太阳能是绿色能源,应大力开发利用 | |
| C. | 核电站是利用原子核聚变所释放的能量来发电 | |
| D. | 火箭发射利用的燃料是液态氢,是因为它含有的热量多 |
20.以下是一些食物的近似pH,对于胃酸过多的人比较适宜吃的食物是( )
| A. | 玉米粥6.8~8.8 | B. | 葡萄3.5~4.5 | C. | 泡菜3.0~4.0 | D. | 橘子2.9~3.5 |
1.在密闭溶液中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应后各物质的质量分数如图所示

下列说法正确的是( )

下列说法正确的是( )
| A. | 丙可能是单质 | |
| B. | 在该反应中丁可能没有参加化学反应 | |
| C. | 该反应是化合反应 | |
| D. | 甲和乙的质量之和一定等于生成丙的质量 |