题目内容
1.学校兴趣小组的同学用不同地点找来的小石块与稀盐酸反应制取二氧化碳.制取二氧化碳的反应化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,各组同学都用了澄清石灰水来检验二氧化碳,反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.小明发现,相邻小组气体产生的速率比自己小组的快,他们对此问题进行了探究.
【提出问题】影响二氧化碳气体产生速率的因素是什么?
【做出猜想】①所用石块大小不同;
②不同地点石块中碳酸钙含量不同;
③还可能是所用盐酸的溶质质量分数(或石块质量不同、盐酸质量不同).
【设计实验】(1)验证猜想①是否成立,要设计的实验:
分别取大小不同、质量相同、相同地点的石块,加入质量相同、溶质质量分数相同的稀盐酸进行实验.
(2)验证猜想②是否成立,对盐酸的要求是质量相同、溶质质量分数相同.
【交流讨论】实验中可以通过观察气泡产生的剧烈程度,粗略地比较反应速率.若要做到精确比较,应该测量的实验数据是相同时间内收集的二氧化碳体积(或收集相同体积二氧化碳所需的时间).
【拓展延伸】上述实验中,小明采用了控制变量的研究方法.若探究“催化剂对用过氧化氢溶液制取氧气的反应速率的影响”时也采用控制变量的研究方法,需要控制不变的因素有温度,溶液的溶质质量分数(或溶液质量、压强)等.
分析 根据碳酸钙和盐酸反应产生氯化钙、水和二氧化碳,氢氧化钙和二氧化碳反应产生碳酸钙沉淀和水,据此书写化学方程式;
【作出猜想】③从药品的表面积和酸的质量分数考虑;
【设计实验】(1)控制不同大小的石块这一个变量;
(2)控制盐酸的溶质质量分数这个变量;
【交流讨论】精确实验结果就要通过准确的数据来证明,故应该准确确定相同时间内二氧化碳的量;
【拓展延伸】从实验所需要的条件的考虑;
解答 解:小石块与稀盐酸反应制取二氧化碳的化学方程式为 CaCO3+2HCl=CaCl2+H2O+CO2↑;澄清石灰水来检验二氧化碳,反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O;
【作出猜想】③影响二氧化碳产生速率的因素还可能是所用盐酸的溶质质量分数(或石块质量不同、盐酸质量不同);
【设计实验】(1)验证猜想①是否成立,要设计的实验:其他量都要相同,但要取产地相同,大小不同的石块,进行实验;
(2)验证猜想②是否成立,对盐酸的要求是质量相同、溶质质量分数相同;
【交流讨论】实验中可以通过观察气泡产生的剧烈程度,粗略地比较反应速率.若要做到精确比较,应该测量的实验数据是相同时间内收集的二氧化碳体积(或收集相同体积二氧化碳所需的时间);
【拓展延伸】探究“催化剂对用过氧化氢溶液制取氧气的反应速率的影响”,需要控制不变的因素有 温度、溶液的溶质质量分数、溶液质量、压强等;
故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑; CO2+Ca(OH)2=CaCO3↓+H2O;
【作出猜想】所用盐酸的溶质质量分数(或石块质量不同、盐酸质量不同);
【设计实验】(1)相同地点;(2)质量相同、溶质质量分数相同;
【交流讨论】相同时间内收集的二氧化碳体积(或收集相同体积二氧化碳所需的时间);
【拓展延伸】温度、溶液的溶质质量分数(或溶液质量、压强).
点评 本题考查了化学反应速率的影响因素,通过控制变量的方法研究化学问题是一种常用的方法,同学们要学会如何控制一个反应的变量,明确哪些变量可以控制等.

| A. | 在演示实验和分组实验中,要力求利用最少的实验药品,获得最佳的实验效果,最大限度的减少废弃物 | |
| B. | 稀释浓硫酸时,应沿杯壁向浓硫酸中缓缓加水,并用玻璃棒不断搅拌 | |
| C. | 取用液体药品时,要把瓶塞反放在桌面上,标签朝向手心,放回原处时标签向外 | |
| D. | 做氢气等可燃气体的燃烧实验时,应先检验气体的纯度后再点燃气体,以防爆炸 | |
| E. | 不能用手接触实验室里的药品,不要凑到容器口闻气体的气味,不能尝药品的味道 | |
| F. | 给试管里的液体加热时,不要把拇指按在短柄上,试管口不能对着自己,试管内液体体积不超过试管容积的一半. |
【提出问题】这包干燥剂是否变质,成分是什么?
【猜想假设】
猜想一:全部是CaO;
猜想二:CaO和Ca(OH)2的混合物;
猜想三:全部是Ca(OH)2;
猜想四:Ca(OH)2和CaCO3的混合物.
【实验探究】
(1)取部分该干燥剂于试管中,加水后无放热现象,说明这包干燥剂中不含CaO;
(2)继续向试管中加入足量稀盐酸,有气泡出现,说明这包干燥剂中含有CaCO3;
(3)为了进一步确定这包干燥剂中有无其它成分,小组同学设计了以下三个方案.另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层清液于三支试管中,请你参与实验,并填写表中的空白
| 实验方案 | 方案一 | 方案二 | 方案三 |
| 实验操作 | 向第一支试管中加入无色酚酞试液 | 向第二支试管中通入CO2气体 | 向第三支试管中加入CuCl2溶液 |
| 实验现象 | 溶液由无色变为红色 | 澄清溶液变浑浊 | 产生蓝色沉淀 |
【实验结论】通过以上实验探究,得出猜想四成立
【拓展迁移】小组同学了解到生石灰做干燥剂的原因是(用化学方程式表示)CaO+H2O═Ca(OH)2;反思了生石灰干燥剂变质的原因,认识到实验室保存生石灰的方法是密封. 碱和盐反应必须是可溶的.写出一种碱和一种盐发生反应的化学方程式.
| A. | Ca2+中的“2”表示一个钙离子带两个单位正电荷 | |
| B. | 2CO中的“2”表示两个一氧化碳分子 | |
| C. | $\stackrel{+2}{Mg}$O中的“2”表示氧化镁中镁元素的化合价为+2价 | |
| D. | O2中的“2”表示两个氧原子 |
| A. | 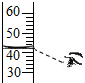 液体读数 | B. | 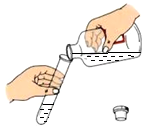 液体取用 | C. | 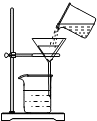 过滤 | D. | 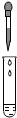 滴加液体 |
 .
.