题目内容
17.生产或生活中蕴含着许多的化学原理,请用化学方程式解释下列原理:(1)工业上利用一氧化碳还原氧化铁炼铁Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)生石灰做干燥剂CaO+H2O=Ca(OH)2.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答 解:(1)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)生石灰是氧化钙的俗称,能与水反应生成氢氧化钙,所以可用来作干燥剂;故填:CaO+H2O=Ca(OH)2.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
5.下列实验方案设计,合理的是( )
| A. | 除去氯化钙溶液中的少量盐酸:加入过量的氧化钙 | |
| B. | 区别固体氯化钙和氯化铵:分别与熟石灰混合研磨 | |
| C. | 制取氢氧化钠溶液:将氢氧化钙溶液与氯化钠溶液混合后过滤 | |
| D. | 检验空气中是否有氧气:将带火星的木条伸入盛有空气的集气瓶中 |
12.分析推理是化学学习中常用的思维方法,下列分析推理正确的是( )
| A. | 复分解反应会生成盐和水,所以生成盐和水的反应一定是复分解反应 | |
| B. | 离子是带电荷的微粒,所以带电荷的微粒一定是离子 | |
| C. | 酸雨的pH小于7,所以pH小7的雨水一定是酸雨 | |
| D. | 氧化还原反应中一定有元素化合价改变,所以复分解反应一定不是氧化还原反应 |
3.废弃电路板中含有大量可利用的塑料、玻璃、金属等物质,利用超临界水技术处理废弃电路板,能得到由CuO和Cu2O组成的固体残渣,将残渣进行进一步处理可得硫酸铜晶体等物质.处理流程如下图所示.下列说法正确的是(已知:Cu2O+H2SO4═CuSO4+Cu+H2O)( )
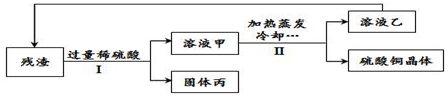

| A. | II中含过滤操作,I中不含 | |
| B. | 溶液甲和溶液乙中均含铜元素 | |
| C. | 残渣的处理流程中,H2SO4和CuSO4实现了循环利用 | |
| D. | 废弃电路板的可回收利用物质中,属于复合材料的是塑料 |
8.下列各项实验,能达到目的是( )
| A. | 用加入适量氯化钡溶液、再过滤的方法,除去硝酸钠溶液中的硫酸钠 | |
| B. | 用加足量水溶解、过滤、蒸发结晶的方法,除去 MnO2固体中 KCl | |
| C. | 用盐酸溶液,验证暴露在空气中的氢氧化钠粉末是否变质 | |
| D. | 用含有稀硝酸的硝酸银溶液,鉴别硫酸钠溶液与氯化钠溶液 |