题目内容
19.为了证明氢氧化钠溶液和硫酸是否发生了反应,小新设计了如下方法进行验证:(1)事先在氢氧化钠溶液中滴入酚酞试剂,然后逐渐滴加硫酸溶液,若观察到溶液由红色变成无色的 现象,则证明氢氧化钠与硫酸发生了反应.
(2)但是小新发现在上述实验中还意外的出现了白色浑浊,经检验氢氧化钠溶液没有混入其他杂质也没有变质,他猜想:可能是酚酞中混入了一种物质,为了验证猜想,他在该酚酞试剂中分别滴加硫酸钠、硫酸钾溶液也都出现白色浑浊,并且加稀硝酸,浑浊不消失.从以上可知小新的猜想是:酚酞中混入了BaCl2(填化学式).
(3)但他很快发现该酚酞试剂中通滴入水也能产生白色浑浊,说明原来的猜想不成立,于是他上网查阅资料:酚酞难溶于水,易溶于酒精,故实验室所用酚酞试液是由酚酞固体溶于酒精配制而成的,于是小新又建立新的猜想,为了验证自己的猜想:小新在常温下用酒精分别配制5份不同浓度的酚酞试剂2毫升,然后分别向5份酚酞试剂中加2毫升蒸馏水,观察实验结果如下:
| 酚酞浓度 | P | $\frac{P}{2}$ | $\frac{P}{4}$ | $\frac{P}{8}$ | $\frac{P}{16}$ |
| 加入蒸馏水后的现象 | 浑浊 | 浑浊 | 澄清 | 澄清 | 澄清 |
根据上表实验现象分析,该酚酞加入其他试剂变浑浊是因为:酚酞浓度过高.
分析 (1)根据酚酞遇碱和中性溶液的变色情况分析解答;
(2)根据加入硫酸钠、硫酸钾都能产生白色沉淀,二者中都含有硫酸根,硫酸钡是不溶于稀硝酸的白色沉淀分析解答;
(3)根据题中数据产生浑浊与酚酞浓度有关进行分析解答.
解答 解:(1)酚酞遇碱变红,氢氧化钠与硫酸发生中和反应生成中性的硫酸钠和水,酚酞遇到中性溶液呈现无色,所以看到的现象是溶液由红色变成无色;
(2)由题中酚酞试液中加入硫酸钠、硫酸钾都能产生不溶于稀硝酸的白色沉淀,能和含有硫酸根的化合物产生不溶于稀硝酸的白色沉淀可能是硫酸钡,所以酚酞中可能含有含有钡离子的盐,如氯化钡或硝酸钡等;
(3)题中表格中信息可知,酚酞溶液浓度不同加入蒸馏水后有不同的现象,溶液越浓变浑浊现象越明显,说明酚酞中加入其他试剂变浑浊的原因是酚酞的浓度过高;
答案:(1)溶液由红色变成无色;(2)BaCl2;(3)酚酞浓度过高.
点评 本题属于信息题的考查,解题的关键要充分利用题目的信息结合控制变量法进行分析对比得出结论,难度较大,能够考查学生的分析问题能力.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
3.今年冬天,雾霾天气肆虐全国许多地方,环境保护是人类共同的责任,下列环境措施中,你认为不可行的是( )
| A. | 大力实施绿化工程防治扬尘污染 | B. | 分类回收垃圾并进行露天焚烧 | ||
| C. | 多使用清洁能源代替煤和石油 | D. | 使用燃煤脱硫技术防治SO2污染 |
7.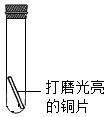 铜片在潮湿的空气中久置,表面会产生绿色的铜锈.某小组同学设计并进行实验,探究铜生锈的条件.
铜片在潮湿的空气中久置,表面会产生绿色的铜锈.某小组同学设计并进行实验,探究铜生锈的条件.
【猜想与假设】常温下,铜生锈可能与O2、CO2、水蒸气有关.
【进行实验】通过控制与铜片接触的物质,利用如图装置(铜片长8cm,宽lcm,试管容积为20mL),分别进行下列7个实验,并持续观察30天.
【解释与结论】
(1)实验3中,要使用经煮沸并迅速泠却的蒸馏水,原因是除去水中的氧气.
(2)实验5的目的是探究铜生锈是否是铜与水和二氧化碳共同反应的结果.
(3)通过上述实验,得出铜生绣的条件是与水、氧气和二氧化碳共同反应.
【反思与评价】
(4)请写出一种防止铜制品锈蚀的方法涂油.
(5)查阅资料可知,铜锈的主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3.由此,你认为上述实验中只需进行实验5、7(填实验编号),就可探究出铜生锈条件,理甶是碱式碳酸铜的化学式中含有碳、氢元素,由元素守恒可以知道,铜生锈的过程中一定有二氧化碳和水参加反应,故只需要进行实验5和7即可知道铜生锈条件是否需要氧气的参加.
(6)与以上进行的实验对比,你认为铜片在通常状况的空气中,生锈非常缓慢的原因可能是空气中氧气、二氧化碳和水蒸气的含量较低.
 铜片在潮湿的空气中久置,表面会产生绿色的铜锈.某小组同学设计并进行实验,探究铜生锈的条件.
铜片在潮湿的空气中久置,表面会产生绿色的铜锈.某小组同学设计并进行实验,探究铜生锈的条件. 【猜想与假设】常温下,铜生锈可能与O2、CO2、水蒸气有关.
【进行实验】通过控制与铜片接触的物质,利用如图装置(铜片长8cm,宽lcm,试管容积为20mL),分别进行下列7个实验,并持续观察30天.
| 编号 | 主要实验操作 | 实验现象 |
| 1 | 充满纯净的O2 | 铜片均无明显变化 |
| 2 | 充满纯净的CO2 | |
| 3 | 充满经煮沸并迅速冷却的蒸馏水 | |
| 4 | 加入蒸馏水5mL (液面未浸没铜片),再充满O2 | |
| 5 | 加入经煮沸并迅速泠却的蒸馏水5ml,再充满CO2 | |
| 6 | 充入10mLO2,再充入10mLCO2 | |
| 7 | 加入蒸馏水5mL,再依次充入l0mLCO2和10mLO2 | 铜片生锈,且水面附近锈蚀最严重 |
(1)实验3中,要使用经煮沸并迅速泠却的蒸馏水,原因是除去水中的氧气.
(2)实验5的目的是探究铜生锈是否是铜与水和二氧化碳共同反应的结果.
(3)通过上述实验,得出铜生绣的条件是与水、氧气和二氧化碳共同反应.
【反思与评价】
(4)请写出一种防止铜制品锈蚀的方法涂油.
(5)查阅资料可知,铜锈的主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3.由此,你认为上述实验中只需进行实验5、7(填实验编号),就可探究出铜生锈条件,理甶是碱式碳酸铜的化学式中含有碳、氢元素,由元素守恒可以知道,铜生锈的过程中一定有二氧化碳和水参加反应,故只需要进行实验5和7即可知道铜生锈条件是否需要氧气的参加.
(6)与以上进行的实验对比,你认为铜片在通常状况的空气中,生锈非常缓慢的原因可能是空气中氧气、二氧化碳和水蒸气的含量较低.
9.硫在空气中燃烧,发出的火焰是( )
| A. | 淡蓝色 | B. | 蓝紫色 | C. | 黄色 | D. | 红色 |

 如图是活性炭净水器示意图,其中活性炭的作用是:吸附色素和异味、滤去不溶性杂质.用此装置得到了澄清透明的水,该水是否为纯水,理由是不是纯水,净化后的水中含有可燃性的杂质.
如图是活性炭净水器示意图,其中活性炭的作用是:吸附色素和异味、滤去不溶性杂质.用此装置得到了澄清透明的水,该水是否为纯水,理由是不是纯水,净化后的水中含有可燃性的杂质.