题目内容
14.实验室有一瓶标签已破损的过氧化氢溶液,同学们为了测定瓶内溶液的溶质质量分数,他们取该溶液34g于烧杯中,加入3gMnO2完全反应后,称得烧杯内剩余物质的总质量为33.8g,请你和他们一起计算:(1)反应后生成氧气的质量是多少?
(2)该瓶过氧化氢溶液中过氧化氢质量是多少?
分析 (1)根据质量守恒定律,反应前后减少的质量为氧气的质量.
(2)利用分解过氧化氢制氧气的化学方程式,根据氧气的质量求出过氧化氢的质量.
解答 解:(1)生成氧气的质量是34g+3g-33.8g=3.2g
(2)该过氧化氢溶液中溶质的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 3.2g
$\frac{68}{32}=\frac{x}{3.2g}$ 解得:x=6.8g
答:(1)反应后生成氧气的质量是3.2g,(2)该瓶过氧化氢溶液中过氧化氢质量是6.8g
点评 本道题目比较简单,是一道最基本的根据化学方程式的计算题,解题关键是根据质量守恒定律求出氧气的质量.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
18.下列有关碳和碳的氧化物的说法中不正确的是( )
| A. | 木炭的燃烧只能生成二氧化碳 | |
| B. | 二氧化碳固体可用于人工降雨 | |
| C. | 一氧化碳能与血液中的血红蛋白结合导致中毒 | |
| D. | 金刚石和石墨都是由碳元素组成的单质 |
19.为了证明氢氧化钠溶液和硫酸是否发生了反应,小新设计了如下方法进行验证:
(1)事先在氢氧化钠溶液中滴入酚酞试剂,然后逐渐滴加硫酸溶液,若观察到溶液由红色变成无色的 现象,则证明氢氧化钠与硫酸发生了反应.
(2)但是小新发现在上述实验中还意外的出现了白色浑浊,经检验氢氧化钠溶液没有混入其他杂质也没有变质,他猜想:可能是酚酞中混入了一种物质,为了验证猜想,他在该酚酞试剂中分别滴加硫酸钠、硫酸钾溶液也都出现白色浑浊,并且加稀硝酸,浑浊不消失.从以上可知小新的猜想是:酚酞中混入了BaCl2(填化学式).
(3)但他很快发现该酚酞试剂中通滴入水也能产生白色浑浊,说明原来的猜想不成立,于是他上网查阅资料:酚酞难溶于水,易溶于酒精,故实验室所用酚酞试液是由酚酞固体溶于酒精配制而成的,于是小新又建立新的猜想,为了验证自己的猜想:小新在常温下用酒精分别配制5份不同浓度的酚酞试剂2毫升,然后分别向5份酚酞试剂中加2毫升蒸馏水,观察实验结果如下:
(注:P是常温下酚酞饱和溶液的浓度)
根据上表实验现象分析,该酚酞加入其他试剂变浑浊是因为:酚酞浓度过高.
(1)事先在氢氧化钠溶液中滴入酚酞试剂,然后逐渐滴加硫酸溶液,若观察到溶液由红色变成无色的 现象,则证明氢氧化钠与硫酸发生了反应.
(2)但是小新发现在上述实验中还意外的出现了白色浑浊,经检验氢氧化钠溶液没有混入其他杂质也没有变质,他猜想:可能是酚酞中混入了一种物质,为了验证猜想,他在该酚酞试剂中分别滴加硫酸钠、硫酸钾溶液也都出现白色浑浊,并且加稀硝酸,浑浊不消失.从以上可知小新的猜想是:酚酞中混入了BaCl2(填化学式).
(3)但他很快发现该酚酞试剂中通滴入水也能产生白色浑浊,说明原来的猜想不成立,于是他上网查阅资料:酚酞难溶于水,易溶于酒精,故实验室所用酚酞试液是由酚酞固体溶于酒精配制而成的,于是小新又建立新的猜想,为了验证自己的猜想:小新在常温下用酒精分别配制5份不同浓度的酚酞试剂2毫升,然后分别向5份酚酞试剂中加2毫升蒸馏水,观察实验结果如下:
| 酚酞浓度 | P | $\frac{P}{2}$ | $\frac{P}{4}$ | $\frac{P}{8}$ | $\frac{P}{16}$ |
| 加入蒸馏水后的现象 | 浑浊 | 浑浊 | 澄清 | 澄清 | 澄清 |
根据上表实验现象分析,该酚酞加入其他试剂变浑浊是因为:酚酞浓度过高.
3.根据反应事实可以推出影响化学反应的因素,下列推理中不合理的是( )
| 选项 | 化学反应事实 | 影响因素 |
| A | 蜡烛在纯氧中燃烧的火焰比在空气中 燃烧的火焰更明亮 | 反应物浓度 |
| B | 煤粉比煤块燃烧得更加剧烈、更加充分 | 反应物种类 |
| C | 木炭在常温下不与氧气反应,点燃时能与氧气反应 | 反应温度 |
| D | 过氧化氢通常情况下难分解,加入二氧化锰后迅速分解 | 催化剂 |
| A. | A | B. | B | C. | C | D. | D |
4.要除去密闭容器内空气中的氧气,可用燃烧除氧气且不产生其它气体和杂质的方法,应选用下列物质中的
( )
( )
| A. | 木炭 | B. | 硫磺 | C. | 白磷 | D. | 蜡烛 |
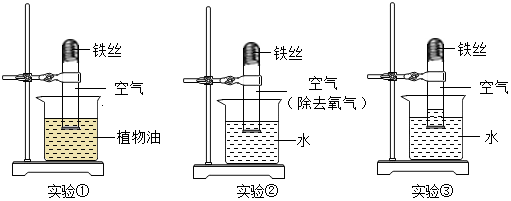
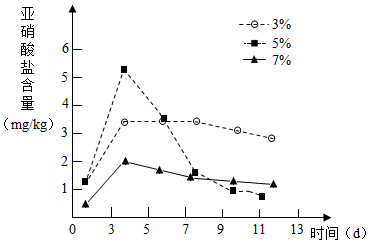 针对泡菜在发酵过程中会产生亚硝酸盐(致癌物质)的事实,某活动小组设计实验,探究不同食盐浓度和发酵时间对亚硝酸盐含量变化的影响,请回答:
针对泡菜在发酵过程中会产生亚硝酸盐(致癌物质)的事实,某活动小组设计实验,探究不同食盐浓度和发酵时间对亚硝酸盐含量变化的影响,请回答: