题目内容
20.联合国气候变化框架公约《京都议定书》要求发达国家限制二氧化碳等温室气体排量,以控制日趋严重的温室效应.(1)绿色植物通过光合作用吸收二氧化碳,放出氧气.
(2)科学家采取“组合转化”技术,将CO2和H2以一定比例混合,在一定条件下反应(反应的化学方程式如下),生成一种重要的化工原料和水.请在括号中填写该化工原料的化学式:2CO2+6H2═C2H4+4H2O
(3)为了减缓大气中CO2含量的增加,以下建议可行的是①③(填序号)
①开发太阳能、水能、风能、地热等新能源;
②禁止使用煤、石油、天然气等矿物燃料;
③大量植树造林,禁止乱砍滥伐.
分析 (1)根据光合作用和呼吸作用的原理作出解答;
(2)根据质量守恒定律化学反应前后原子的种类和数目都不变确定化学式;
(3)减缓大气中CO2含量的增加的思路一是减小排放、二是增加二氧化碳的消耗.
解答 解:(1)植物光合作用的原理是吸收二氧化碳放出氧气,而呼吸作用的原是吸收氧气放出二氧化碳;
(2)根据质量守恒定律化学反应前后原子的种类和数目都不变,反应生成的这种化工原料的一个分子中含有两个碳原子和四个氢原子,其化学式为C2H4,
故答案为:C2H4;
(3)了减缓大气中CO2含量的增加的主要方法一是开发利用新的清洁的能源,减少化石能源的利用.二是加大植树造林的力度,提高二氧化碳的吸收能力,
故选①③.
答案:
(1)光合;二氧化碳;氧气;
(2)C2H4;
(3)①③.
点评 本题考查环境污染及治理,侧重于化学与人体健康的考查,为高考常见题型和高频考点,有利于培养学生的良好科学素养,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
5.化学兴趣小组同学发现实验台上按如图所示顺序摆放着6瓶不同的无色溶液(如图所示:A、B、C、D、E、F代表对应的溶液).其中E溶液的试剂瓶标签破损.为此,他们做了如下探究:

【提出问题】E溶液的成分是什么?
【初步判断】根据受损标签及实验室药品分类摆放原则,E溶液不可能是①(填序号).
①酸;②碱;③盐.
【提出猜想】猜想Ⅰ:NaOH溶液;猜想Ⅱ:Na2CO3溶液;猜想Ⅲ:Na2SO4溶液;猜想Ⅳ:NaCl溶液(任写一种).
【设计并实验】兴趣小组的同学为验证“猜想Ⅱ”是否正确,设计并完成如表所示实验.
【分析与推理】
①完成“实验一”后,李成同学即认为“猜想Ⅰ”正确,张平同学认为“猜想Ⅰ”不一定正确,他的理由是因NaOH溶液变质也会产生Na2CO3不合理.
②请写出“实验三”中发生反应的化学方程式Na2CO3+BaCl2=2NaCl+BaCO3↓.
【反思与评价】
经过讨论,同学们认为“实验一”存在明显操作错误,该错误是把pH试纸浸入待测液;观察发现D、E试剂瓶的瓶塞是橡胶塞.

【提出问题】E溶液的成分是什么?
【初步判断】根据受损标签及实验室药品分类摆放原则,E溶液不可能是①(填序号).
①酸;②碱;③盐.
【提出猜想】猜想Ⅰ:NaOH溶液;猜想Ⅱ:Na2CO3溶液;猜想Ⅲ:Na2SO4溶液;猜想Ⅳ:NaCl溶液(任写一种).
【设计并实验】兴趣小组的同学为验证“猜想Ⅱ”是否正确,设计并完成如表所示实验.
| 实验方案 | 实验一 | 实验二 | 实验三 |
| 实验操作 |  |  |  |
| 实验现象 | 试纸变色,对照比色卡,pH>7 | 有无色无味气体产生 | 有白色沉淀产生 |
| 实验结论 | 猜想Ⅱ正确 | ||
①完成“实验一”后,李成同学即认为“猜想Ⅰ”正确,张平同学认为“猜想Ⅰ”不一定正确,他的理由是因NaOH溶液变质也会产生Na2CO3不合理.
②请写出“实验三”中发生反应的化学方程式Na2CO3+BaCl2=2NaCl+BaCO3↓.
【反思与评价】
经过讨论,同学们认为“实验一”存在明显操作错误,该错误是把pH试纸浸入待测液;观察发现D、E试剂瓶的瓶塞是橡胶塞.



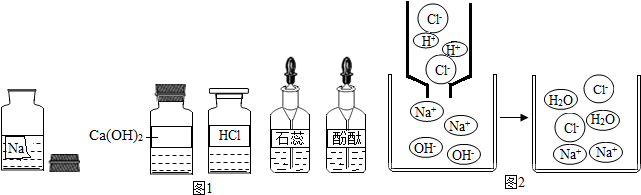 【提出问题】这瓶溶液是什么溶液?
【提出问题】这瓶溶液是什么溶液?