题目内容
19.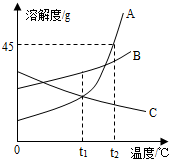 如图是A、B、C三种物质的溶解度曲线,根据此图回答下列问题:
如图是A、B、C三种物质的溶解度曲线,根据此图回答下列问题:(1)t1℃时,物质A和C的溶解度相等.
(2)t2℃时,A物质的溶解度是45g.
(3)等质量的A、B、C三种物质的饱和溶液同时从t2℃降温到t1℃,其中溶质质量分数没有发生改变的是C.
(4)t2℃时,小红向100g的水中加入45.8gA物质,她发现A物质全部溶解,一段时间后,她意外地发现又有部分A物质的晶体析出.我认为A物质“全部溶解”的原因是因为A物质溶解时放热(填“吸热”或“放热”)引起;析出晶体的原因是温度降低,A物质的溶解度变小.
分析 根据题目信息和溶解度曲线可知:A、B两种固体物质的溶解度,都是随温度升高而增大,而C的溶解度随温度的升高而减少;t1℃时,物质A和C的溶解度相等;t2℃时,A物质的溶解度是45g;等质量的A、B、C三种物质的饱和溶液同时从t2℃降温到t1℃,其中溶质质量分数没有发生改变的是C,因为C的溶解度随温度的升高而减少,只是由饱和变为不饱和,质量分数不变;A物质“全部溶解”的原因是因为A物质溶解时,放热引起;析出晶体的原因是:温度降低,A物质的溶解度变小.
解答 解:(1)由溶解度曲线可知:t1℃时,物质A和C的溶解度相等,故答案为:t1;
(2)由溶解度曲线可知:t2℃时,A物质的溶解度是45g;故答案为:45
(3)等质量的A、B、C三种物质的饱和溶液同时从t2℃降温到t1℃,其中溶质质量分数没有发生改变的是C,因为C的溶解度随温度的升高而减少,只是由饱和变为不饱和,质量分数不变;故答案为:C
(4)A物质“全部溶解”的原因是因为A物质溶解时,放热引起;析出晶体的原因是:温度降低,A物质的溶解度变小;故答案为:放热;温度降低,A物质的溶解度变小;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目
12.某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应的生成物,通过查阅资料知道::①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$CO↑+CO2↑+H2O.
②NaOH溶液可以吸收二氧化碳,
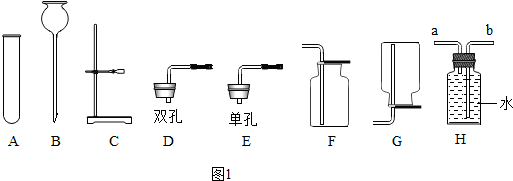
③常温下,Ca(OH)2微溶于水;于是他设计了如图1的实验装置,结合装置回答下列问题:
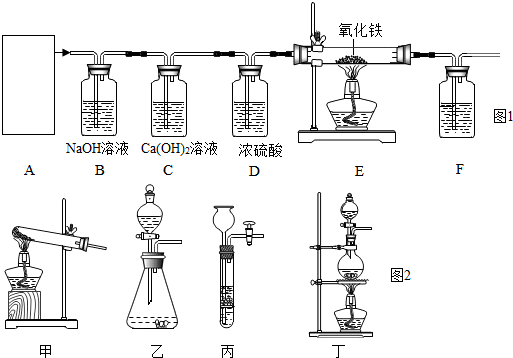
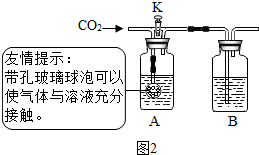
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择图2中的丁(填装置编号);
(2)图中装置C、D的作用分别是判断二氧化碳是否被氢氧化钠溶液完全吸收、干燥一氧化碳气体;
(3)该装置设计有一个明显缺陷,你认为是没有处理尾气.
(4)实验时准确称取一定质量纯净的Fe2O3固体按图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却.将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生.
查阅资料:a.铁的氧化物在足量的稀盐酸中均能全部溶解.
b.Fe2O3与CO反应的固体生成物可能情况如下:Fe2O3$\stackrel{400℃~500℃}{→}$Fe3O4$\stackrel{500℃~600℃}{→}$$\underset{FeO}{黑色}$$\stackrel{700℃~800℃}{→}$Fe
根据“无气泡”猜想,黑色粉末可能是:①Fe3O4;②FeO;③Fe3O4、FeO
(5)定量分析,用电子天平称量得部分数据如下:
根据上述数据,推断出反应后黑色固体的成分是Fe3O4.
②NaOH溶液可以吸收二氧化碳,
③常温下,Ca(OH)2微溶于水;于是他设计了如图1的实验装置,结合装置回答下列问题:

(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择图2中的丁(填装置编号);
(2)图中装置C、D的作用分别是判断二氧化碳是否被氢氧化钠溶液完全吸收、干燥一氧化碳气体;
(3)该装置设计有一个明显缺陷,你认为是没有处理尾气.
(4)实验时准确称取一定质量纯净的Fe2O3固体按图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却.将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生.
查阅资料:a.铁的氧化物在足量的稀盐酸中均能全部溶解.
b.Fe2O3与CO反应的固体生成物可能情况如下:Fe2O3$\stackrel{400℃~500℃}{→}$Fe3O4$\stackrel{500℃~600℃}{→}$$\underset{FeO}{黑色}$$\stackrel{700℃~800℃}{→}$Fe
根据“无气泡”猜想,黑色粉末可能是:①Fe3O4;②FeO;③Fe3O4、FeO
(5)定量分析,用电子天平称量得部分数据如下:
| 玻璃管质量 | 玻璃管及其中固体的质量 | 装置F及其中物质的总质量 | |
| 反应前 | 28.20g | 33.00g | 300.0g |
| 反应后 | 32.84g | 300.4g |
7.某同学在实验室进行了木炭还原氧化铜的实验,实验步骤如下:
⑤为确定木炭还原氧化铜后的固体成分,请你与兴趣小组的同学完成以下探究(注:该反应还原产物只有铜).
【猜想】猜想Ⅰ:全部都是金属铜; 猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭; 猜想Ⅳ:除铜外,还含有氧化铜、木炭.
【实验与结论】待试管冷却后将剩余固体倒入烧杯,加入足量稀硫酸,过滤,得到蓝色滤液,
滤渣为红色和黑色固体混合物.证明猜想猜想Ⅳ成立;写出氧化铜与稀硫酸反应的化学方程式CuO+H2SO4═CuSO4+H2O.
【实验反思】混合物中仍含有氧化铜的原因可能是碳和氧化铜没有完全反应就停止了加热,或者还可能的原因是从试管B中撤出导管时,有空气进入试管,与灼热的铜再次反应生成氧化铜.
| 实验装置 | 实验步骤 | 分析 |
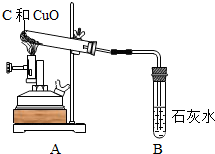 | ①检验装置气密性 | |
| ②把木炭和氧化铜的混合物放入试管,如左图所示连接实验装置 | 装置中存在的问题是B试管处不应该有橡皮塞 | |
| ③改进装置后,点燃酒精喷灯开始实验 | 装置B的作用是检验产物是否有二氧化碳 | |
| ④反应结束时,先将导管从装置B中撤出,再停止加热 | 目的是防止液体倒流引起试管炸裂 |
【猜想】猜想Ⅰ:全部都是金属铜; 猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭; 猜想Ⅳ:除铜外,还含有氧化铜、木炭.
【实验与结论】待试管冷却后将剩余固体倒入烧杯,加入足量稀硫酸,过滤,得到蓝色滤液,
滤渣为红色和黑色固体混合物.证明猜想猜想Ⅳ成立;写出氧化铜与稀硫酸反应的化学方程式CuO+H2SO4═CuSO4+H2O.
【实验反思】混合物中仍含有氧化铜的原因可能是碳和氧化铜没有完全反应就停止了加热,或者还可能的原因是从试管B中撤出导管时,有空气进入试管,与灼热的铜再次反应生成氧化铜.
4.下列图示实验操作中,正确的是( )
| A. |  | B. |  | C. | 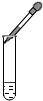 | D. |  |