题目内容
11.在托盘天平两端各放一只等质量的烧杯,向两只烧杯中分别注入相同质量、相同质量分数的稀硫酸,天平平衡.向左盘烧杯中加入镁,右盘烧杯中加入铁,反应完毕后,天平仍然平衡,则加入镁和铁的质量比可能是①81:77 ②7:3 ③3:7 ④1:1( )
| A. | ①② | B. | ①④ | C. | ③ | D. | ③④ |
分析 天平仍然平衡,说明溶液增加的质量相等,据此可得出本题的答案.
解答 解:第一种情况:加入的两种金属都完全反应:
设镁的质量为x,铁的质量为y,溶液增加的质量为z.
Mg+H2SO4=MgSO4+H2↑ 增加的质量
24 2 24-2=22
x z
$\frac{24}{x}=\frac{22}{z}$
x=$\frac{12z}{11}$
Fe+H2SO4=FeSO4+H2↑ 增加的质量
56 2 56-2=54
y z
$\frac{56}{y}=\frac{54}{z}$
y=$\frac{28z}{27}$
加入镁和铁的质量比为 $\frac{12z}{11}:\frac{28z}{27}$=81:77.
第二种情况,金属过量:
则生成氢气与硫酸质量有关,氢气质量相等,由于天平平衡,所以m(硫酸)+m(铁)-m(铁生成的氢气)=m(硫酸)+m(镁)-m(镁产生的氢气),由于硫酸和氢气质量相等,所以m(铁)=m(镁).所以加入的金属质量是相等的.
故选B.
点评 本题主要考查有关化学方程式的计算,难度较大.关键是要将溶液增加的质量作为得到答案的桥梁.题目没有说明金属必须是相等等条件,所以存在各种可能性.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
4.青少年正处在身体发育时期,一定要注意营养均衡,不可挑食偏食.下列营养物质中不能产生人体所需能量的是( )
| A. |  新鲜牛奶 | B. |  土豆 | C. |  花生油 | D. |  食盐 |
2. 某电镀厂的电镀液中含有金盐,为了回收其中的金元素,技术人员制作了如图的“吸金球”,“吸金球”是装入一些“吸金”物质的纱袋,把“吸金球”浸入电镀液,能“吸”出盐溶液中的金,据上所述,“吸金球”中的“吸金”物质可能是( )
某电镀厂的电镀液中含有金盐,为了回收其中的金元素,技术人员制作了如图的“吸金球”,“吸金球”是装入一些“吸金”物质的纱袋,把“吸金球”浸入电镀液,能“吸”出盐溶液中的金,据上所述,“吸金球”中的“吸金”物质可能是( )
 某电镀厂的电镀液中含有金盐,为了回收其中的金元素,技术人员制作了如图的“吸金球”,“吸金球”是装入一些“吸金”物质的纱袋,把“吸金球”浸入电镀液,能“吸”出盐溶液中的金,据上所述,“吸金球”中的“吸金”物质可能是( )
某电镀厂的电镀液中含有金盐,为了回收其中的金元素,技术人员制作了如图的“吸金球”,“吸金球”是装入一些“吸金”物质的纱袋,把“吸金球”浸入电镀液,能“吸”出盐溶液中的金,据上所述,“吸金球”中的“吸金”物质可能是( )| A. | 活性炭(C) | B. | 铁屑(Fe) | ||
| C. | 硫酸铜(CuSO4) | D. | 磁石(主要成分是Fe3O4) |
6.下列实验对应现象的描述错误的是( )
| A. | 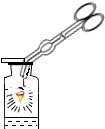 铁丝在氧气中燃烧:剧烈燃烧,火星四射,放出大量的热.产生黑色固体 | |
| B. | 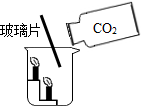 二氧化碳缓缓倒入放有高低两支燃着的蜡烛的烧杯里:下层的蜡烛火焰先熄灭,上层的蜡烛火焰后熄灭 | |
| C. | 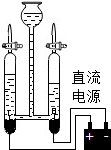 电解水的实验:两个电极上产生大量的气泡,正极上产生的是氢气,负极上产生的是氧气 | |
| D. | 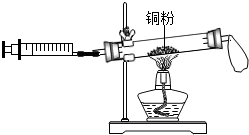 测定空气成分的实验:玻璃管内红色的固体粉末变成黑色,气体的总体积减少了约1/5 |
16. 随着经济的发展,能源与环境成为人们日益关注的问题.
随着经济的发展,能源与环境成为人们日益关注的问题.
(1)6月5日是世界环境日,下列有关环境与能源的说法错误的是ABD.
A.焚烧塑料是减少白色污染的有效方法
B.目前氢能源没有广泛推广的主要原因是淡水资源缺乏
C.空气中O3含量超标会引起温室效应
D.化工厂可通过加高烟囱排放废气,防止空气污染
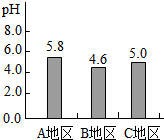
(2)酸雨是由SO2、NO2等气体或这些气体在空气中反应后的生成物溶于雨水所形成.A、B、C三个地区雨水的pH如图所示,其中BC地区的雨水是酸雨.
(3)人们正在利用和开发其他能源,如太阳能、风能等.
(4)下面是煤的一种综合利用方式.在一定条件下,甲+乙→丙+丁.甲乙丙丁分别表示四种物质,它们的部分化学式和微观示意图分别列于表:
①写出甲物质的化学式H2O,画出丁物质的微观示意图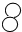 .
.
②构成丙物质的粒子是分子(填“分子”、“原子”或“离子”).
 随着经济的发展,能源与环境成为人们日益关注的问题.
随着经济的发展,能源与环境成为人们日益关注的问题.(1)6月5日是世界环境日,下列有关环境与能源的说法错误的是ABD.
A.焚烧塑料是减少白色污染的有效方法
B.目前氢能源没有广泛推广的主要原因是淡水资源缺乏
C.空气中O3含量超标会引起温室效应
D.化工厂可通过加高烟囱排放废气,防止空气污染
(2)酸雨是由SO2、NO2等气体或这些气体在空气中反应后的生成物溶于雨水所形成.A、B、C三个地区雨水的pH如图所示,其中BC地区的雨水是酸雨.
(3)人们正在利用和开发其他能源,如太阳能、风能等.
(4)下面是煤的一种综合利用方式.在一定条件下,甲+乙→丙+丁.甲乙丙丁分别表示四种物质,它们的部分化学式和微观示意图分别列于表:
| 物质 | 甲 | 乙 | 丙 | 丁 | 图例: |
| 化学式 | ? | C | ? | H2 | |
| 微观 示意图 |  |  |  | ? |
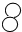 .
.②构成丙物质的粒子是分子(填“分子”、“原子”或“离子”).
3.实验是学习化学的重要途径,以下小涛的实验操作中正确的是( )
| A. | 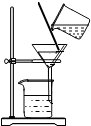 过滤 | B. | 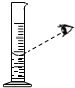 读取液体的体积 | C. |  测量溶液的PH | D. | 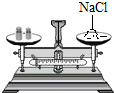 称量食盐 称量食盐 |
20.建立宏微观和符号之间的联系是化学学科的特点
(1)在水、铜和氯化钠3中物质中,构成氯化钠的基本微粒是离子(填“分子”、“原子”或“离子”).
(2)军事上用于制造隐形飞机涂层的四硫富瓦烯(C6H4S4)汽油吸收微波的功能.四硫富瓦烯属于有机物(填“有机物”或“无机物”)
(3)A、B、C、D表示4种物质,其微观示意图见下表.A和B在一定条件下反应可生成C和D.根据图示回答下列问题.
①1个D分子中含有2个原子;
②对于该反应,下列所发正确的是ac(填字母序号).
a.4种物质均由分子构成
b.反应前后各元素化合价均发生改变
c.4种物质中属于氧化物的是A、B、C
d.C、D两种物质的质量比为11:7.
(1)在水、铜和氯化钠3中物质中,构成氯化钠的基本微粒是离子(填“分子”、“原子”或“离子”).
(2)军事上用于制造隐形飞机涂层的四硫富瓦烯(C6H4S4)汽油吸收微波的功能.四硫富瓦烯属于有机物(填“有机物”或“无机物”)
(3)A、B、C、D表示4种物质,其微观示意图见下表.A和B在一定条件下反应可生成C和D.根据图示回答下列问题.
| 反应前 | 反应后 |  | ||
| A | B | C | D | |
 |  |  |  | |
②对于该反应,下列所发正确的是ac(填字母序号).
a.4种物质均由分子构成
b.反应前后各元素化合价均发生改变
c.4种物质中属于氧化物的是A、B、C
d.C、D两种物质的质量比为11:7.
19.同学们运用对比的学习方法探究碱的性质.
(1)由如图实验一、二可知,氢氧化钠会吸收空气的二氧化碳、水,因此要密封保存.
(2)实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C,A瓶内发生反应的化学方程式为CO2+2NaOH=Na2CO3+H2O,对比A瓶与C(选填“B”或“C”)瓶的实验现象可证明CO2能与NaOH发生反应.
(3)同学们设计如下两种方案鉴别饱和氢氧化钠溶液与饱和氢氧化钙溶液(分别编号为A、B).
实验一 | 实验二 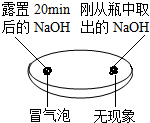 | 实验三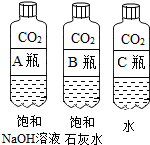 |
| 观察固体表面 | 向两块固体表面滴加稀盐酸 | 振荡三个塑料瓶 |
(2)实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C,A瓶内发生反应的化学方程式为CO2+2NaOH=Na2CO3+H2O,对比A瓶与C(选填“B”或“C”)瓶的实验现象可证明CO2能与NaOH发生反应.
(3)同学们设计如下两种方案鉴别饱和氢氧化钠溶液与饱和氢氧化钙溶液(分别编号为A、B).
| 方案一 | 方案二 | 分析 |
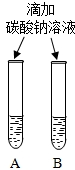 | 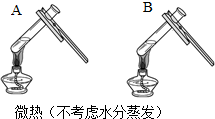 | 两种方案中均观察到A试管内出现白色浑浊,A中试剂为饱和氢氧化钙溶液; 方案二的A溶液变浑浊的原因是氢氧化钙的溶解度随温度升高而减少;氢氧化钠的溶解度随温度升高而升高;两者的溶解度受温度影响情况不同 |
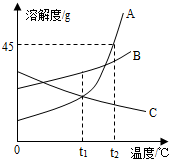 如图是A、B、C三种物质的溶解度曲线,根据此图回答下列问题:
如图是A、B、C三种物质的溶解度曲线,根据此图回答下列问题: