题目内容
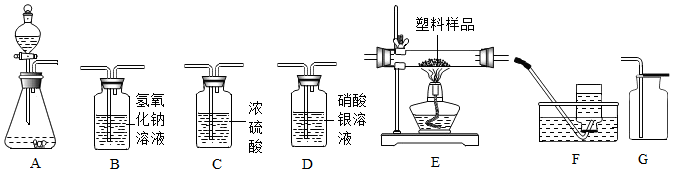
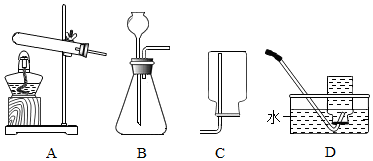
14.请根据下列装置图回答问题.
(1)A中制取气体的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,其验满的方法是将燃着的木条接近瓶口,观察火焰是否熄灭. A装置还可用于实验室制取氧气,反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)实验B中,观察到蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是密度大于空气,不能燃烧,不能支持燃烧.
分析 (1)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,二氧化碳不具有助燃性,过氧化氢在二氧化锰的催化作用下分解生成水和氧气进行分析;
(2)根据实验B中,蜡烛自下而上依次熄灭的现象进行分析.
解答 解:(1)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,二氧化碳不具有助燃性,所以验满的方法是:将燃着的木条接近瓶口,观察火焰是否熄灭,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)实验B中,蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是:密度大于空气,不能燃烧,不能支持燃烧.
故答案为:(1)CaCO3+2HCl=CaCl2+H2O+CO2↑,将燃着的木条接近瓶口,观察火焰是否熄灭,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)密度大于空气,不能燃烧,不能支持燃烧.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.日常生活中人们常喝纯净水,市场上出售的纯净水有一些是蒸馏水.对于这一类纯净水的下列说法,正确的是( )
| A. | 它容易导电 | |
| B. | 它适合于家庭养金鱼 | |
| C. | 它含有人体所需的矿物质和多种微量元素 | |
| D. | 它清洁、纯净,但长期饮用对健康无益 |
5.下列各组金属中,按金属活动性由强到弱的顺序排列正确的是( )
| A. | K Al Zn | B. | Zn Na Hg | C. | Fe Zn Al | D. | Mg Ca Cu |
9.下列实际应用中,利用中和反应原理的是( )
①用生石灰作食品干燥剂
②用熟石灰和硫酸铜配制波尔多液
③施用熟石灰改良酸性土壤
④用氢氧化钠溶液处理泄漏的浓硫酸
⑤碳酸钠中和面团中过多的酸.
①用生石灰作食品干燥剂
②用熟石灰和硫酸铜配制波尔多液
③施用熟石灰改良酸性土壤
④用氢氧化钠溶液处理泄漏的浓硫酸
⑤碳酸钠中和面团中过多的酸.
| A. | ②⑤ | B. | ③④ | C. | ①④⑤ | D. | ②③ |
19.下列物质的俗名、化学名称和化学式相一致的是( )
| A. | 生石灰、氧化钙、CaO | B. | 纯碱、氢氧化钠、NaOH | ||
| C. | 石灰石、氢氧化钙、Ca(OH)2 | D. | 熟石灰、碳酸钙、CaCO3 |
4.小明已通过基础实验6-“粗盐的提纯”除去了难溶性杂质,查阅资料发现,实验得到的“精盐”中还含有MgCl2、Na2SO4和CaCl2可溶性杂质,他称取了一定量的“精盐”,并设计了如下实验流程再进行除杂提纯,进一步得到较纯净的NaCl固体,下列做法正确的是( )
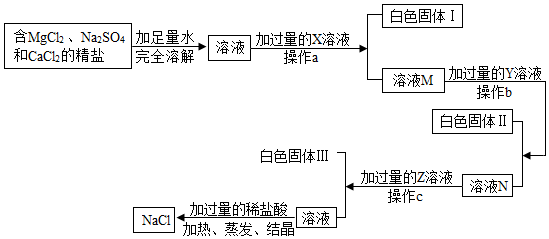

| A. | 操作a、操作b和操作c相同,都为过滤 | |
| B. | 若X、Y、Z分别为NaOH、BaCl2、Na2CO3,则溶液N中的溶质为CaCl2 | |
| C. | 若Z为Na2CO3,则白色固体一定为BaCO3和CaCO3 | |
| D. | 加入过量的稀盐酸的目的是除去过量的Na2CO3 |