题目内容
12. 某同学对蜡烛及其燃烧进行了如下探究.请填写下列空格.
某同学对蜡烛及其燃烧进行了如下探究.请填写下列空格.①取一支蜡烛,用小刀切下一小块,把它放入水中,蜡烛浮在水面上.结论:石蜡的密度比水小.
②点燃蜡烛,观察到蜡烛火焰分为外焰、内焰、焰心三层.把一根火柴梗放在蜡烛的火焰中(如图)约1s后取出可以看到火柴梗的a处最先碳化.
结论:蜡烛火焰的外焰层温度最高.
③再将一只干燥的烧杯罩在蜡烛火焰上方,烧杯内壁出现水雾,结论:石蜡燃烧后生成了水.取下烧杯,迅速向烧杯内倒人少量澄清的石灰水,振荡,澄清石灰水变浑浊.结论:石蜡燃烧后还生成了二氧化碳.据此写出蜡烛燃烧的文字表达式石蜡+氧气$\stackrel{点燃}{→}$二氧化碳+水.
分析 ①根据蜡烛能浮在水面上,比较蜡烛和水的密度;
②根据温度越高,火柴梗易被炭化分析;
③将一只干燥的烧杯罩在蜡烛火焰上方,烧杯内壁出现水雾,说明有水生成;迅速向烧杯内倒入少量澄清石灰水,振荡,澄清石灰水变浑浊,说明生成了二氧化碳;据此结合质量守恒定律,进行分析解答.
解答 解:①由于蜡烛浮在水面上,说明石蜡的密度比水小且不溶于水;
②蜡烛火焰分为外焰、内焰、焰心三层;由于温度越高,火柴梗易被炭化,所以,看到火柴梗的c处最先变黑,说明蜡烛火焰的外焰温度最高;
③将一只干燥的烧杯罩在蜡烛火焰上方,烧杯内壁出现水雾,说明有水生成;迅速向烧杯内倒入少量澄清石灰水,振荡,澄清石灰水变浑浊,说明生成了二氧化碳;石蜡与氧气在点燃的条件下反应生成二氧化碳和水.
故答案为:①小;②外焰、内焰、焰心;a;外焰;③水;二氧化碳;石蜡+氧气$\stackrel{点燃}{→}$二氧化碳+水.
点评 本题难度不大,考查蜡烛燃烧的现象,掌握蜡烛燃烧的现象、注意事项等是正确解答本题的关键.

练习册系列答案
相关题目
17.我们生活在物质的世界里,而物质在不断地变化.下列四个变化中,与其他三个变化有本质区别的是( )
| A. | 铁生锈 | B. | 蜡烛燃烧 | C. | 加热高锰酸钾 | D. | 工业制取氧气 |
4.小明已通过基础实验6-“粗盐的提纯”除去了难溶性杂质,查阅资料发现,实验得到的“精盐”中还含有MgCl2、Na2SO4和CaCl2可溶性杂质,他称取了一定量的“精盐”,并设计了如下实验流程再进行除杂提纯,进一步得到较纯净的NaCl固体,下列做法正确的是( )
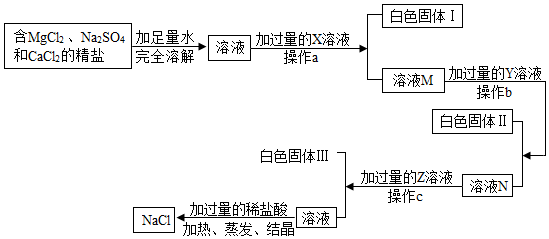

| A. | 操作a、操作b和操作c相同,都为过滤 | |
| B. | 若X、Y、Z分别为NaOH、BaCl2、Na2CO3,则溶液N中的溶质为CaCl2 | |
| C. | 若Z为Na2CO3,则白色固体一定为BaCO3和CaCO3 | |
| D. | 加入过量的稀盐酸的目的是除去过量的Na2CO3 |
2.聪聪做镁条在空气中燃烧实验时发现除生成白色固体外还有少量淡黄色固体,他对得到的固体成分进行探究.
【提出问题】固体成分是什么?
【提出猜想】猜想一:MgO
猜想二:Mg3 N2
猜想三:MgO、Mg3N2
【查阅资料】MgO与水反应类似于CaO与水反应;Mg3N2与水反应产生NH3.
【表达与交流】聪聪在老师的指导下,用定量的方法确定猜想三正确,请写出将固体投入水中相关反应的化学方程式.CaO+H2O═Ca(OH)2、Mg3N2+6H2O=3Mg(OH)2+2NH3↑.
【想关结论】空气中N2和O2体积比约为4:1,由镁条在空气中燃烧生成少量Mg3N2可得出的一个结论是氮气含量多但是很稳定,难以发生反应.
【提出问题】固体成分是什么?
【提出猜想】猜想一:MgO
猜想二:Mg3 N2
猜想三:MgO、Mg3N2
【查阅资料】MgO与水反应类似于CaO与水反应;Mg3N2与水反应产生NH3.
| 实验操作 | 实验现象 | 实验结论 |
| 将该固体投入到盛水的烧杯中 | 若烧杯中只有白色固体,无刺激性气味气体产生 | 猜想一正确 |
烧杯底部有白色固体,有刺激性气味气体生成 | 猜想二或猜想三正确 |
【想关结论】空气中N2和O2体积比约为4:1,由镁条在空气中燃烧生成少量Mg3N2可得出的一个结论是氮气含量多但是很稳定,难以发生反应.
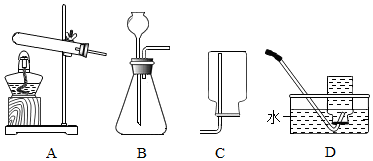
 下面是一学习小组采用下列装置进行科学探究提出的几个问题,请将下列问题补充完整.
下面是一学习小组采用下列装置进行科学探究提出的几个问题,请将下列问题补充完整.