题目内容
19.如图1是甲、乙、丙三种固体的溶解度曲线,试回答:(1)t3℃时,甲的溶解度为90g;t3℃时,甲、乙、丙三种物质溶解度的由大到小的顺序是甲=乙>丙.
(2)t2℃时,甲物质形成的饱和溶液中溶质与溶剂的质量比为1:2.
(3)t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液中溶质质量分数由小到大的顺序是丙<甲<乙,析出固体质量关系为甲>乙(填“>”、“=”或“<”).
(4)t2℃时,将30g甲物质加入到50g水中充分溶解,所形成溶液的质量是75g.
(5)t2℃时,要使接近饱和的甲溶液变为该温度下的饱和溶液,可采取的方法是加溶质或蒸发溶剂.
(6)从含有少量甲的乙溶液中提纯乙的方法是蒸发结晶.
(7)t3℃时,若将50g的甲物质加入到100g水中,充分溶解后,所得的溶液在溶解度曲线图中可表示为B(“A、”“B”、“C”)点,若将该溶液降温至t2℃,溶液的变化情况是a、d.
a.溶液变为饱和b.溶解度增加c.溶液减少d.溶液的质量分数不变
(8)t2℃时,将含有100g水的甲的饱和溶液变为t3℃时甲的饱和溶液,采取的方法是加溶质、减少溶剂.
(9)某同学在t1℃时开始如图2实验,得到相应的溶液.

在溶液①--⑤中,属于饱和溶液的是②④⑤.
在溶液②溶质质量分数相等的是⑤.
烧杯④中所得溶液的质量为150g.
烧杯⑤中固体的质量为30g.
(10)下表是KNO3和NaCl在不同温度下的溶解度:
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | ■ |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | ■ |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | ■ |
②对①析出的晶体和剩余溶液描述正确的是A(填写编号).
A.剩余溶液一定是KNO3饱和溶液
B.剩余溶液一定是NaCl不饱和溶液
C.上述方法可以将两者完全分离
D.析出的晶体中一定只含有KNO3
③在一定温度下,将含69gKNO3、18gNaCl的混合物完全溶解在50g水中.欲使KNO3析出,NaCl不析出,则温度T(℃)的范围是20℃~70℃(硝酸钾和氯化钠溶解度互不影响).
分析 根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而丙的溶解度随温度的升高而减少;t3℃时,甲的溶解度为90g;t3℃时,甲、乙、丙三种物质溶解度的由大到小的顺序是:甲=乙>丙;t2℃时,甲物质形成的饱和溶液中溶质与溶剂的质量比=50g:100g=1:2;t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液中溶质质量分数由小到大的顺序是:丙<甲<乙,因为甲析出结晶比乙多,丙由饱和溶液变成不饱和溶液,质量分数还是最小;t2℃时,将30g甲物质加入到50g水中充分溶解,所形成溶液的质量=25g+50g=75g;t2℃时,要使接近饱和的甲溶液变为该温度下的饱和溶液,可采取的方法是:加溶质,蒸发溶剂;从含有少量甲的乙溶液中提纯乙的方法是:蒸发结晶,因为乙的溶解度受温度的变化不大;t3℃时,若将50g的甲物质加入到100g水中,充分溶解后,所得的溶液在溶解度曲线图中可表示为B点,若将该溶液降温至t2℃,溶液的变化情况是:由不饱和溶液变成饱和溶液、溶液的质量分数不变;t2℃时,将含有100g水的甲的饱和溶液变为t3℃时甲的饱和溶液,采取的方法是:加溶质、减少溶剂.在溶液①--⑤中,属于饱和溶液的是②④⑤,属于不饱和溶液的是①③;在溶液②溶质质量分数相等的是⑤,都是t1℃时的饱和溶液;烧杯④中所得溶液的质量=50g+100g=150g;烧杯⑤中固体的质量为30g.KNO3溶液中含有少量NaCl时,可通过降温结晶的方法提纯硝酸钾,因为硝酸钾受温度的影响比较大;对①析出的晶体和剩余溶液描述正确的是:剩余溶液一定是KNO3饱和溶液;在一定温度下,将含69gKNO3、18gNaCl的混合物完全溶解在50g水中.欲使KNO3析出,NaCl不析出,则温度T(℃)的范围是:20℃~70℃.
解答 解:(1)t3℃时,甲的溶解度为90g;t3℃时,甲、乙、丙三种物质溶解度的由大到小的顺序是:甲=乙>丙;故答案为:90g;甲=乙>丙;
(2)t2℃时,甲物质形成的饱和溶液中溶质与溶剂的质量比=150g:100g=3:2;故答案为:3:2;
(3)t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液中溶质质量分数由小到大的顺序是:丙<甲<乙,因为甲析出结晶比乙多,丙由饱和溶液变成不饱和溶液,质量分数还是最小;故答案为:丙<甲<乙;>;
(4)t2℃时,将30g甲物质加入到50g水中充分溶解,所形成溶液的质量=25g+50g=75g;故答案为:75;
(5)t2℃时,要使接近饱和的甲溶液变为该温度下的饱和溶液,可采取的方法是:加溶质,蒸发溶剂;故答案为:加溶质;蒸发溶剂;
(6)从含有少量甲的乙溶液中提纯乙的方法是:蒸发结晶,因为乙的溶解度受温度的变化不大;故答案为:蒸发结晶;
(7)t3℃时,若将50g的甲物质加入到100g水中,充分溶解后,所得的溶液在溶解度曲线图中可表示为B点,若将该溶液降温至t2℃,溶液的变化情况是:由不饱和溶液变成饱和溶液、溶液的质量分数不变;故答案为:B;ad;
(8)t2℃时,将含有100g水的甲的饱和溶液变为t3℃时甲的饱和溶液,采取的方法是:加溶质、减少溶剂;故答案为:加溶质、减少溶剂;
(9)在溶液①--⑤中,属于饱和溶液的是②④⑤,属于不饱和溶液的是①③;在溶液②溶质质量分数相等的是⑤,都是t1℃时的饱和溶液;烧杯④中所得溶液的质量=50g+100g=150g;烧杯⑤中固体的质量为30g;故答案为:②④⑤;⑤;150;30;
(10)KNO3溶液中含有少量NaCl时,可通过降温结晶的方法提纯硝酸钾,因为硝酸钾受温度的影响比较大;对①析出的晶体和剩余溶液描述正确的是:剩余溶液一定是KNO3饱和溶液;在一定温度下,将含69gKNO3、18gNaCl的混合物完全溶解在50g水中.欲使KNO3析出,NaCl不析出,则温度T(℃)的范围是:20℃~70℃;故答案为:降温结晶;A;20℃~70;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案| A. | 它由10个原子构成 | B. | 它的摩尔质量为74g | ||
| C. | 1molC3H6S中约含6.02×1024个原子 | D. | 其中碳、氢、硫元素质量比为3:6:1 |
| A. | 百事可乐 | B. | 食用豆油 | C. | 苛性钠 | D. | 加碘食盐 |
| A. |  O2验满 | B. |  收集氧气 | C. | 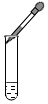 滴加液体 | D. |  称量氯化钠固体 |
 有一瓶标签残缺的无色溶液如图所示.
有一瓶标签残缺的无色溶液如图所示.【提出问题】该溶液的溶质是什么?
【分析问题】根据老师的介绍及试剂的存放规律,该溶液的溶质可能是Na2CO3、NaOH、或NaHCO3中的一种
【查阅资料】20℃时几种物质的溶解度如表:
| 物质 | Na2CO3 | NaOH | NaHCO3 |
| 溶解度(g) | 20 | 40 | 10 |
(1)通过分析该溶液一定不是NaHCO3,理由是20℃时,饱和碳酸氢钠溶液的溶质质量分数小于10%;
(2)该溶液到底是什么,请完成实验设计:
| 操作步骤 | 观察到的现象 | 结论 |
| 取溶液少量于试管中加适量的氯化钙溶液 | 出现白色沉淀 | 该溶液是碳酸钠溶液 |
(4)能否用酚酞试液判断溶质的种类,理由是不能,碳酸钠溶液和氢氧化钠溶液都显碱性,都能使酚酞试液变红色.
【反思】造成试剂瓶标签破损的原因,从实验操作及药品性质分析可能是倾倒液体时标签没有向着手心,流下时腐蚀了标签.
