题目内容
14.用化学用语表示:(1)空气中含量最多的分子N2;
(2)生物细胞中含量最多的物质H2O;
(3)硫酸铜溶液的阳离子Cu2+;
(4)8个氨气分子8NH3;
(5)氧化铁中铁元素为+3价$\stackrel{+3}{Fe}$2O3.
分析 (1)空气中含量最多的气体是氮气,氮气是由氮分子构成的,进行分析解答.
(2)生物细胞中含量最多的物质是水,写出其化学式即可.
(3)硫酸铜溶液的阳离子是铜离子,写出其离子符号即可.
(4)分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字.
(5)化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后.
解答 解:(1)空气中含量最多的气体是氮气,氮气是由氮分子构成的,空气中含量最多的分子是氮分子,其分子符号为:N2.
(2)生物细胞中含量最多的物质是水,其化学式为:H2O.
(3)硫酸铜溶液的阳离子是铜离子,其离子符号为:Cu2+.
(4)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则8个氨分子可表示为:8NH3.
(5)由化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后,故氧化铁中铁元素为+3价可表示为:$\stackrel{+3}{Fe}$2O3.
故答案为:(1)N2;(2)H2O;(3)Cu2+;(4)8NH3;(5)$\stackrel{+3}{Fe}$2O3.
点评 本题难度不大,掌握常见化学用语(分子符号、化学式、化合价、离子符号等)的书写方法、离子符号与化合价表示方法的区别等是正确解答此类题的关键.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
5.K2CO3是常用的钾肥,其焰色反应呈( )
| A. | 红色 | B. | 黄色 | C. | 紫色 | D. | 绿色 |
6.水是生命之源,水与我们的生活息息相关.下列与水有关的说法正确的是( )
| A. | 水电解产生氢气和氧气,说明分子中含有氢分子和氧分子 | |
| B. | 实验室里为了节约用自来水配置溶液 | |
| C. | 常用肥皂水来检验硬水和软水 | |
| D. | 过滤可以除去水中所有的杂质 |
2.下列说法中错误的是( )
| A. | 在化学变化中分子改变,原子不变 | |
| B. | 在化学变化中分子改变,物理变化中分子不变 | |
| C. | 分子能保持物质的物理性质 | |
| D. | 化学反应前后分子的个数一定不变 |
9.化学学习小组做实验时记录了下列实验现象,其中不正确的是( )
| A. | 少量高锰酸钾固体溶于水可得到紫红色溶液 | |
| B. | 红热的木炭在氧气中燃烧时,发出白光 | |
| C. | 细铁丝伸入盛有氧气的集气瓶中剧烈燃烧 | |
| D. | 向酚酞溶液中逐滴加入氨水,液体颜色由无色变成红色 |
19.如图1是甲、乙、丙三种固体的溶解度曲线,试回答:
(1)t3℃时,甲的溶解度为90g;t3℃时,甲、乙、丙三种物质溶解度的由大到小的顺序是甲=乙>丙.
(2)t2℃时,甲物质形成的饱和溶液中溶质与溶剂的质量比为1:2.
(3)t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液中溶质质量分数由小到大的顺序是丙<甲<乙,析出固体质量关系为甲>乙(填“>”、“=”或“<”).
(4)t2℃时,将30g甲物质加入到50g水中充分溶解,所形成溶液的质量是75g.
(5)t2℃时,要使接近饱和的甲溶液变为该温度下的饱和溶液,可采取的方法是加溶质或蒸发溶剂.
(6)从含有少量甲的乙溶液中提纯乙的方法是蒸发结晶.
(7)t3℃时,若将50g的甲物质加入到100g水中,充分溶解后,所得的溶液在溶解度曲线图中可表示为B(“A、”“B”、“C”)点,若将该溶液降温至t2℃,溶液的变化情况是a、d.
a.溶液变为饱和b.溶解度增加c.溶液减少d.溶液的质量分数不变
(8)t2℃时,将含有100g水的甲的饱和溶液变为t3℃时甲的饱和溶液,采取的方法是加溶质、减少溶剂.
(9)某同学在t1℃时开始如图2实验,得到相应的溶液.

在溶液①--⑤中,属于饱和溶液的是②④⑤.
在溶液②溶质质量分数相等的是⑤.
烧杯④中所得溶液的质量为150g.
烧杯⑤中固体的质量为30g.
(10)下表是KNO3和NaCl在不同温度下的溶解度:
①KNO3溶液中含有少量NaCl时,可通过降温结晶的方法提纯.
②对①析出的晶体和剩余溶液描述正确的是A(填写编号).
A.剩余溶液一定是KNO3饱和溶液
B.剩余溶液一定是NaCl不饱和溶液
C.上述方法可以将两者完全分离
D.析出的晶体中一定只含有KNO3
③在一定温度下,将含69gKNO3、18gNaCl的混合物完全溶解在50g水中.欲使KNO3析出,NaCl不析出,则温度T(℃)的范围是20℃~70℃(硝酸钾和氯化钠溶解度互不影响).
(1)t3℃时,甲的溶解度为90g;t3℃时,甲、乙、丙三种物质溶解度的由大到小的顺序是甲=乙>丙.
(2)t2℃时,甲物质形成的饱和溶液中溶质与溶剂的质量比为1:2.
(3)t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液中溶质质量分数由小到大的顺序是丙<甲<乙,析出固体质量关系为甲>乙(填“>”、“=”或“<”).
(4)t2℃时,将30g甲物质加入到50g水中充分溶解,所形成溶液的质量是75g.
(5)t2℃时,要使接近饱和的甲溶液变为该温度下的饱和溶液,可采取的方法是加溶质或蒸发溶剂.
(6)从含有少量甲的乙溶液中提纯乙的方法是蒸发结晶.
(7)t3℃时,若将50g的甲物质加入到100g水中,充分溶解后,所得的溶液在溶解度曲线图中可表示为B(“A、”“B”、“C”)点,若将该溶液降温至t2℃,溶液的变化情况是a、d.
a.溶液变为饱和b.溶解度增加c.溶液减少d.溶液的质量分数不变
(8)t2℃时,将含有100g水的甲的饱和溶液变为t3℃时甲的饱和溶液,采取的方法是加溶质、减少溶剂.
(9)某同学在t1℃时开始如图2实验,得到相应的溶液.

在溶液①--⑤中,属于饱和溶液的是②④⑤.
在溶液②溶质质量分数相等的是⑤.
烧杯④中所得溶液的质量为150g.
烧杯⑤中固体的质量为30g.
(10)下表是KNO3和NaCl在不同温度下的溶解度:
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | ■ |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | ■ |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | ■ |
②对①析出的晶体和剩余溶液描述正确的是A(填写编号).
A.剩余溶液一定是KNO3饱和溶液
B.剩余溶液一定是NaCl不饱和溶液
C.上述方法可以将两者完全分离
D.析出的晶体中一定只含有KNO3
③在一定温度下,将含69gKNO3、18gNaCl的混合物完全溶解在50g水中.欲使KNO3析出,NaCl不析出,则温度T(℃)的范围是20℃~70℃(硝酸钾和氯化钠溶解度互不影响).
3.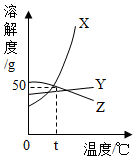 如图是X、Y、Z三种物质的溶解度曲线.下列说法正确的是( )
如图是X、Y、Z三种物质的溶解度曲线.下列说法正确的是( )
 如图是X、Y、Z三种物质的溶解度曲线.下列说法正确的是( )
如图是X、Y、Z三种物质的溶解度曲线.下列说法正确的是( )| A. | 溶解度变化受温度影响最大的是Y | |
| B. | t℃时,饱和Z溶液中溶质质量分数为50% | |
| C. | 要想从X、Y的混合溶液中分离出物质X可以冷却热饱和溶液 | |
| D. | t℃时,要想降低三种物质饱和溶液的溶质质量分数均可采用添加溶剂和升高温度的方法 |
4.下列关于碳及碳的化合物说法正确的是( )
| A. | C→CO2的转化,可以通过燃烧实现 | |
| B. | 金刚石和石墨都是碳单质,都具有良好的导电性 | |
| C. | 二氧化碳有毒,因此进入久未开启的菜窖之前,必须先做灯火试验 | |
| D. | 除去CO2中的少量CO可通过点燃的方法 |