题目内容
11.用所学知识回答下列问题.(1)水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解一些有关水的知识.请你回答:
①天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是蒸馏;
②硬水给生活和生产带来很多麻烦,生活中可用肥皂水来区分硬水和软水,生活中常用煮沸的方法来降低水的硬度;
③地球上的总储水量虽然很大,但淡水很少,爱护水资源是每个公民的责任和义务.
下列行为属于节约用水的是ABD.(填字母)
A.公共场所随手关水龙头 B.洗完菜的水用来浇花
C.不间断放水刷牙 D.“中水”用于洗车或用于城市绿化
(2)配制溶质质量分数一定的氯化钠溶液是初中化学重要的实验.现需要50g质量分数为10%的氯化钠溶液.请回答下列问题:
①若用氯化钠固体配制,需称取氯化钠5g.
②如图所示的序号表示正确配制氯化钠溶液的操作顺序为CBDEA.(填字母)

③用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应B(填字母).
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节游码 D.添加砝码.
分析 (1)①根据不同的净化操作的净化程度进行分析判断;
②根据区分硬水和软水常用的方法是用肥皂水,根据日常生活软化硬水的方法进行解答;
③根据节约用水的常用措施进行分析;
(2)①根据溶质质量=溶液质量×溶质质量分数进行分析;
②根据配制氯化钠溶液的制取操作步骤进行分析;
③根据天平称量固体的正确操作方法进行分析.
解答 解:(1)①根据净水的原理、方法可知,蒸馏得到的水为纯水,所以蒸馏的净化程度最高;
②硬水和软水的区别在于所含的钙镁离子的多少,生活中可用肥皂水来区分硬水和软水,产生泡沫较多的是软水,较少的硬水;生活中常用煮沸的方法来降低水的硬度;
③A、公共场所随手关水龙头,这是节约水的做法,可取,故A正确;
B、洗完菜的水用来浇花,这种做法能提高水的利用率,可节约用水,可取,故B正确;
C、不间断放水刷牙,这会浪费水,故C错误;
D、用“中水”用于洗车或用于城市绿化,可以节约水资源,故D正确.
故选ABD;
(2)①需称取氯化钠为:50g×10%=5g;
②配制氯化钠溶液的制取操作步骤有:计算、称量、溶解、装瓶,所以正确配制氯化钠溶液的操作顺序为CBDEA;
③用托盘天平称量所需的氯化钠,氯化钠是固定的,发现托盘天平的指针偏向左盘,说明氯化钠多了,需要减少氯化钠,故选B.
故答案为:(1)①蒸馏;
②肥皂水,煮沸;
③ABD;
(2)①5g;
②CBDEA;
③B.
点评 本题难度不大,了解净化水的常用方法、硬水与软水的检验与转化方法等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列实验过程与图象相符的是( )
| A. | 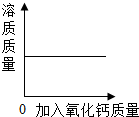 一定温度下,向饱和的石灰水中加入氧化钙固体 一定温度下,向饱和的石灰水中加入氧化钙固体 | |
| B. | 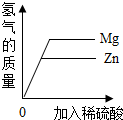 向等量的镁、锌固体中加入足量的稀硫酸 向等量的镁、锌固体中加入足量的稀硫酸 | |
| C. | 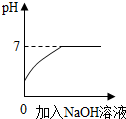 向稀盐酸中加入过量的氢氧化钠溶液 向稀盐酸中加入过量的氢氧化钠溶液 | |
| D. | 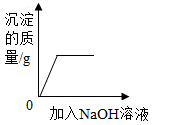 向盐酸和氯化镁混合溶液中加入过量的氢氧化钠溶液 向盐酸和氯化镁混合溶液中加入过量的氢氧化钠溶液 |
6.柠檬酸(C6H8O7)是一种常见的有机酸,存在于多种水果中,常用于配制饮料等、柠檬酸在水中可以解离出来H+,从而呈现酸性.下列物质不能与柠檬酸反应的是( )
| A. | Zn | B. | CuO | C. | CO2 | D. | Ca(OH)2 |
16.下列应用及相应原理(用化学方程式表示)及基本反应类型都正确的是( )
| A. | 用木炭测空气中氧气含量C+02$\frac{\underline{\;点燃\;}}{\;}$C02化合反应 | |
| B. | 高炉炼铁中发生的主要反应2Fe203+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3C02↑ 置换反应 | |
| C. | 用稀盐酸除铁锈 Fe203+6HCI=2FeCl3+3H20 复分解反应 | |
| D. | 实验室制二氧化碳 CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ 分解反应 |
3.向AgNO3、Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤,向滤液中滴加稀盐酸有白色沉淀产生.下列说法中,正确的是( )
| A. | 所得滤渣中一定含有铜和锌 | |
| B. | 所得滤渣中一定含有银和铜 | |
| C. | 所得滤渣中一定含有银、铜和锌 | |
| D. | 所得滤液中一定含有Ag+、Zn2+、Cu2+ |
 如图所示,实验Ⅱ是电解水的装置.
如图所示,实验Ⅱ是电解水的装置.
