题目内容
18.实验室用大理石和稀盐酸反应测定某大理石样品中碳酸钙的质量分数.向烧杯中加入9g大理石粉末,再加入50g(过量)溶质质量为14.6%的稀盐酸,杂质不与稀盐酸反应.充分反应后烧杯中剩余物质的质量为55.7g,求该大理石样品中碳酸钙的质量分数.(结果保留到0.1%)分析 首先根据质量守恒定律求出生成的二氧化碳的质量即反应前后物质总质量的差值,然后把二氧化碳的质量代入化学方程式计算就可求出参加反应的碳酸钙的质量,碳酸钙的质量与大理石的质量的百分比即为大理石样品中碳酸钙的质量分数.
解答 解:根据质量守恒定律可得,生成的二氧化碳的质量是50g+9g-55.7g=3.3g;
设大理石样品中碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 3.3g
$\frac{100}{x}=\frac{44}{3.3g}$
x=7.5g
大理石样品中碳酸钙的质量分数为:$\frac{7.5g}{9g}$×100%=83.3%
答:大理石样品中碳酸钙的质量分数为83.3%.
点评 本题难度不是很大,主要考查了质量守恒定律的应用和根据化学方程式进行有关的计算,培养学生分析问题的能力和解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.现有20%的硫酸溶液50 克,把它配成10%的硫酸溶液,应选用的一组仪器是( )
| A. | 托盘天平、量筒、玻璃棒 | B. | 量筒、烧杯、玻璃棒 | ||
| C. | 托盘天平、量筒、烧杯 | D. | 托盘天平、烧杯、玻璃棒 |
13.模型法是化学研究的重要方法之一,二氧化碳的分子模型可表示为 ,其中○表示氧原子,●表示碳原子,从模型图不能获得的信息是( )
,其中○表示氧原子,●表示碳原子,从模型图不能获得的信息是( )
 ,其中○表示氧原子,●表示碳原子,从模型图不能获得的信息是( )
,其中○表示氧原子,●表示碳原子,从模型图不能获得的信息是( )| A. | 一个二氧化碳分子由几个原子构成 | B. | 二氧化碳分子由什么原子构成 | ||
| C. | 二氧化碳分子的空间结构 | D. | 一个分子和一个原子的真实大小 |
3.下列关于实验操作的描述不正确的是( )
| A. | 做细铁丝在氧气中燃烧的实验时,集气瓶内要预留少量水 | |
| B. | 稀释浓硫酸时,将浓硫酸沿内壁缓缓注入盛有水烧杯中 | |
| C. | 做一氧化碳还原氧化铁实验时,先通一氧化碳后加热 | |
| D. | 测定溶液酸碱度时,直接将pH试纸伸入待测溶液中 |
7.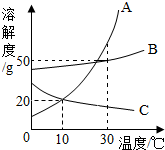 如图是A、B、C三种固体物质的溶解度曲线,下列说法不正确的是( )
如图是A、B、C三种固体物质的溶解度曲线,下列说法不正确的是( )
 如图是A、B、C三种固体物质的溶解度曲线,下列说法不正确的是( )
如图是A、B、C三种固体物质的溶解度曲线,下列说法不正确的是( )| A. | 30℃时,A、B、C三种物质的溶解度曲线由大到小的顺序是:A>B>C | |
| B. | 30℃时,A、B、C三种饱和溶液同时降温到10℃,所得溶液中溶质分数由大到小的顺序是:B>A>C | |
| C. | 10℃时,A、B、C三种饱和溶液同时升温到30℃,所得溶液中溶质分数由大到小的顺序是:B>A>C | |
| D. | 30℃时,A、B、C三种饱和溶液同时降温到10℃,析出的晶体质量大到小的顺序一定是:A>B>C |