题目内容
3.以下改进实验能够更好地达成实验目的.| 图1:验证CO2的性质 | 图2:用H2O2和MnO2制O2 | 图3:探究可燃物燃烧的条件 |
 |  |  |
②按图2所示进行实验可以制取氧气,用启普发生器制取氧气的优点是可随时控制反应的发生和停止(写一点),
写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
③图3实验证明了可燃物燃烧的条件之一为可燃物燃烧温度需达到着火点,写出白磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
④待图3实验结束后,将甲试管从烧杯中取出并按下图进行实验.若白磷足量,理论上进入试管中的水的体积约占试管容积的$\frac{1}{5}$.

分析 ①根据实验的现象分析二氧化碳的性质;
②根据启普发生器特点分析;
③根据白磷燃烧的现象及燃烧的条件分析;
④根据氧气约占空气体积的$\frac{1}{5}$,可以完成该题的解答.
解答 解:(1)在实验1中,把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层蜡烛先灭,说明二氧化碳的密度比空气大、不燃烧和不支持燃烧的性质;
(2)启普发生器可随时控制反应的发生和停止;过氧化氢在二氧化锰的催化下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)白磷燃烧,红磷不燃烧;可得燃烧的条件为可燃物燃烧温度需达到着火点.白磷燃烧的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;由于空气总氧气约占空气体积的$\frac{1}{5}$,如果白磷足量、气密性良好,试管中的氧气能消耗完,所以进入a试管内液体的体积能接近试管容积的 $\frac{1}{5}$.
故答案为:①密度比空气大、不能燃烧、不能支持燃烧;②可随时控制反应的发生和停止;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;③可燃物燃烧温度需达到着火点;4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;$\frac{1}{5}$.
点评 本题考查知识点的方式比较灵活,但并不是难题,同学们只要掌握二氧化碳的物理、化学性质以及与燃烧条件的实验就可以顺利完成该题,解题的关键是理清其中的转化关系.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
13.下列物质的用途主要由物理性质决定的是( )
| A. | 镁粉用于制作照明弹 | B. | 金刚石用来制作玻璃刀 | ||
| C. | 氢气用于作清洁燃料 | D. | 氮气用作焊接金属时的保护气 |
11.鱼类食物富含铁,此处“铁”指的是( )
| A. | 元素 | B. | 原子 | C. | 分子 | D. | 单质 |
18.将饱和硝酸钾溶液转化为不饱和溶液的方法是( )
| A. | 加水 | B. | 降温 | C. | 蒸发水 | D. | 加溶质 |
8. 水是地球上一种最普通、最常见的物质.
水是地球上一种最普通、最常见的物质.
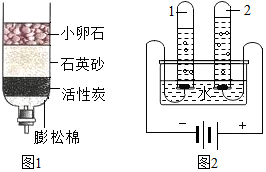
①图1所示的是简易净水器,其中活性炭的作用是过滤和吸附.
②水厂处理水时,有时会向水中加生石灰,此过程中发生的化学方程式为CaO+H2O═Ca(OH)2.
③图2是电解水的简易装置,试管1中生成的气体是氢气,反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
④将少量下面的调味品加入水中,不能形成溶液的是D.
A.食盐B.蔗糖C.味精D.芝麻油
⑤碘酒中的溶剂为酒精(质名称)
⑥在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液.加入KNO3固体的质量与所得溶液的质量如下表:
①实验a、b、c、d中,有未被溶解的KNO3固体析出的实验是d(填写实验编号).
②该温度下KNO3的溶解度是110g.
③实验a、b、c、d所得溶液中质量分数大小关系为:a<b<c=d.
④取实验b所得溶液,若使其质量分数变为20%,在不改变温度的情况下,可以采取的操作是加入150g水.
 水是地球上一种最普通、最常见的物质.
水是地球上一种最普通、最常见的物质.①图1所示的是简易净水器,其中活性炭的作用是过滤和吸附.
②水厂处理水时,有时会向水中加生石灰,此过程中发生的化学方程式为CaO+H2O═Ca(OH)2.
③图2是电解水的简易装置,试管1中生成的气体是氢气,反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
④将少量下面的调味品加入水中,不能形成溶液的是D.
A.食盐B.蔗糖C.味精D.芝麻油
⑤碘酒中的溶剂为酒精(质名称)
⑥在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液.加入KNO3固体的质量与所得溶液的质量如下表:
| 实验编号 | a | b | c | d |
| 加入KNO3固体的质量 | 45 | 50 | 55 | 60 |
| 所得溶液的质量 | 95 | 100 | 105 | 105 |
②该温度下KNO3的溶解度是110g.
③实验a、b、c、d所得溶液中质量分数大小关系为:a<b<c=d.
④取实验b所得溶液,若使其质量分数变为20%,在不改变温度的情况下,可以采取的操作是加入150g水.
15.图示的四个图象分别对应四个变化过程的一种趋势,下列分析正确的是( )
| A. | 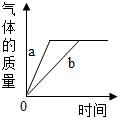 可能是双氧水溶液制氧气,a未使用催化剂,b使用了催化剂 | |
| B. | 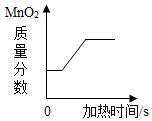 可能是加热一定质量的氯酸钾和二氧化锰固体混合物制取氧气过程 | |
| C. | 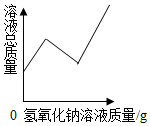 可能是硫酸铜溶液中滴加氢氧化钠溶液 | |
| D. | 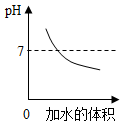 可能是向一定量的氢氧化钠溶液中加水稀释,溶液的pH变化 |

 阅读下面科普短文(原文作者高存文、王晶禹,原文有删改).
阅读下面科普短文(原文作者高存文、王晶禹,原文有删改).