题目内容
14. 甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:(1)25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为65g.
(2)将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数不变(填“变大”、“变小”或“不变”).
(3)要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是加入甲物质(或恒温蒸发溶剂).
(4)向100g35℃的水中加入45g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出.你认为“全部溶解”的原因可能是甲固体溶于水时放热.
分析 (1)根据25℃时甲物质的溶解度分析解答;
(2)根据丙的溶解度随温度降低而增大分析解答;
(3)根据不饱和溶液与饱和溶液的转化方法分析解答;
(4)根据甲的溶解度随温度的变化情况分析解答.
解答 解:(1)25℃时,甲物质的溶解度是30g,即100g水中最多溶30g,则50g水中最多溶15g,所得溶液质量为:15g+50g=65g;
(2)将35℃时丙的饱和溶液降温到25℃,丙的溶解度变大,溶液由饱和变为不饱和,没有晶体析出,溶液中溶质、溶剂的质量不变,故溶质质量分数不变;
(3)接近饱和的溶液变成饱和,可以用加入溶质和恒温蒸发溶剂、降温的方法,因为温度不变,所以不能采取降温的方法;
(4)因为甲的溶解度随温度的升高而增大,所以开始发现全部溶解,一段时间后又有部分甲的晶体析出说明甲物质溶于水放热,开始温度升高,溶解度增大,冷却后溶液温度降低,溶解度变小,析出晶体;
故答案为:(1)65;(2)不变;(3)加入甲物质(或恒温蒸发溶剂);(4)甲固体溶于水时放热.
点评 解答本题的关键是要知道溶解度曲线表示的意义,溶质质量分数的计算方法,饱和溶液与不饱和溶液的相互转化等知识,才能结合题意灵活分析解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.下列物质的名称(或俗称)、化学式、分类均正确的是( )
| A. | 硫酸铁 FeSO4 盐 | B. | 纯碱 NaOH 碱 | ||
| C. | 熟石灰 CaO 氧化物 | D. | 乙醇 C2H5OH 有机物 |
2.某固体混合物由K2CO3、K2SO4、CaCl2和KCl中的一种或几种组成,实验记录如下:
①取该样品溶于水,得到无色溶液;
②取适量上述溶液加过量的BaCl2溶液,出现白色沉淀,过滤;
③向步骤②所得沉淀中加入过量的稀HNO3,沉淀部分消失并产生气泡;
④取步骤②的溶液加人AgNO3溶液生成白色沉淀,再加入稀HNO3,振荡,沉淀不消失.
下列分析正确的是( )
①取该样品溶于水,得到无色溶液;
②取适量上述溶液加过量的BaCl2溶液,出现白色沉淀,过滤;
③向步骤②所得沉淀中加入过量的稀HNO3,沉淀部分消失并产生气泡;
④取步骤②的溶液加人AgNO3溶液生成白色沉淀,再加入稀HNO3,振荡,沉淀不消失.
下列分析正确的是( )
| A. | 原固体混合物中一定不含有CaCl2、KCl | |
| B. | 原固体混合物中一定含有K2CO3、K2SO4、KCl | |
| C. | 只通过步骤①②就可以确定原固体混合物中一定含有K2SO4 | |
| D. | 若步骤②改为滴加过量的Ba(NO3)2溶液,其余操作及现象均不变,则原固体混合物中一定含有KCl |
6.如图所示的微观变化与下列反应及反应类型对应正确的是( )


| A. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 化合反应 | B. | 2HI+Cl2═2HCl+I2 置换反应 | ||
| C. | 2H2O $\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ 分解反应 | D. | 2HCl+CuO═CuCl2+H2O 复分解反应 |
3. 如图是地壳中元素质量分数的模型图,其中A代表的元素是( )
如图是地壳中元素质量分数的模型图,其中A代表的元素是( )
 如图是地壳中元素质量分数的模型图,其中A代表的元素是( )
如图是地壳中元素质量分数的模型图,其中A代表的元素是( )| A. | 铝元素 | B. | 氧元素 | C. | 钙元素 | D. | 氢元素 |
4.按下列要求书写的化学方程式正确的是( )
| A. | 镁在氧气中燃烧:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| B. | 用电解水的方法测定水的组成2H20=2H2↑+O2↑ | |
| C. | 在密闭容器中燃烧白磷验证质量守恒定律4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | |
| D. | 用稀硫酸清洗试管内壁附着的铜Cu+H2SO4=CuSO4+H2↑ |
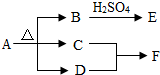 铜锈A[Cu2(OH)2CO3]在加热条件下得到B、C、D三种氧化物,如图所示.将固体B溶入足量稀硫酸中得到溶液E,将气体C通入D中得到溶液F.请回答下列问题:
铜锈A[Cu2(OH)2CO3]在加热条件下得到B、C、D三种氧化物,如图所示.将固体B溶入足量稀硫酸中得到溶液E,将气体C通入D中得到溶液F.请回答下列问题: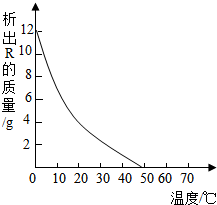 溶液在生产和科研中具有广泛的用途,与人们的生活密不可分.
溶液在生产和科研中具有广泛的用途,与人们的生活密不可分.