题目内容
4.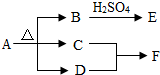 铜锈A[Cu2(OH)2CO3]在加热条件下得到B、C、D三种氧化物,如图所示.将固体B溶入足量稀硫酸中得到溶液E,将气体C通入D中得到溶液F.请回答下列问题:
铜锈A[Cu2(OH)2CO3]在加热条件下得到B、C、D三种氧化物,如图所示.将固体B溶入足量稀硫酸中得到溶液E,将气体C通入D中得到溶液F.请回答下列问题:(1)B→E的实验现象是黑色固体逐渐消失,溶液由无色变成蓝色,化学方程式是CuO+H2SO4=CuSO4+H2O.
(2)气体C通入D中化学方程式是H2O+CO2=H2CO3,溶液F中含有的分子有H2O、CO2、H2CO3.
分析 根据碱式碳酸铜在加热的条件下生成氧化铜、水和二氧化碳,B会与硫酸反应,所以B是氧化铜,C、D是水和二氧化碳,氧化铜和硫酸反应生成硫酸铜和水,所以E是硫酸铜,水和二氧化碳反应生成碳酸,所以F是碳酸,然后将推出的物质进行验证即可.
解答 解:(1)碱式碳酸铜在加热的条件下生成氧化铜、水和二氧化碳,B会与硫酸反应,所以B是氧化铜,C、D是水和二氧化碳,氧化铜和硫酸反应生成硫酸铜和水,所以E是硫酸铜,水和二氧化碳反应生成碳酸,所以F是碳酸,经过验证,推导正确,所以B→E的实验现象是:黑色固体逐渐消失,溶液由无色变成蓝色,化学方程式为:CuO+H2SO4=CuSO4+H2O;
(2)气体C通入D中化学方程式是:H2O+CO2=H2CO3,溶液F中含有的分子有H2O、CO2、H2CO3.
故答案为:(1)黑色固体逐渐消失,溶液由无色变成蓝色,CuO+H2SO4=CuSO4+H2O;
(2)H2O+CO2=H2CO3,H2O、CO2、H2CO3.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
14.某化学兴趣小组为了探究铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行了如下探究活动:
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀的致密氧化膜.铬能与稀硫酸反应,生成氢气和硫酸铬(CrSO4)
【提出猜想】对这三种金属的活动性顺序提出了如下猜想:
猜想①:Cr>Al>Cu猜想②:Cr>Cu>Al 猜想③:Al>Cr>Cu 猜想④:Al>Cu>Cr
【讨论交流】根据已学的金属活动性顺序和已查阅的资料分析,肯定不能成立的是猜想②和猜想④(填序号).
【实验设计及过程】请将表中的内容填写完整.
【实验反思】
(1)将金属片投入稀硫酸前应先打磨金属片的目的是A.
A.除去金属表面氧化物,有利于直接反应
B.使金属表面光亮,便于观察现象
C.使金属表面温度升高,提高反应温度
(2)有同学提出探究金属活动性强弱还可以依据“金属与金属化合物溶液是否发生置换反应”来判断.为了验证甲、乙、丙三种金属的活动性依次减弱,某同学设计了如下方案:①把甲放入乙的化合物溶液中②把乙放入丙的化合物溶液中③把甲放入丙的化合物溶液中.你认为该方案中的③(填序号)没有必要做.
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀的致密氧化膜.铬能与稀硫酸反应,生成氢气和硫酸铬(CrSO4)
【提出猜想】对这三种金属的活动性顺序提出了如下猜想:
猜想①:Cr>Al>Cu猜想②:Cr>Cu>Al 猜想③:Al>Cr>Cu 猜想④:Al>Cu>Cr
【讨论交流】根据已学的金属活动性顺序和已查阅的资料分析,肯定不能成立的是猜想②和猜想④(填序号).
【实验设计及过程】请将表中的内容填写完整.
| 实验操作 | 实验现象 | 实验结论 |
| 室温下,将大小相同并打磨光亮的铬片、铝片、铜片分别浸入盛有体积相同、溶质质量分数相同的稀硫酸的试管中. | 铬片表面产生气泡缓慢,铝片表面产生气泡较快,铜片表面没有气泡. | 猜想③ (填序号)成立. |
(1)将金属片投入稀硫酸前应先打磨金属片的目的是A.
A.除去金属表面氧化物,有利于直接反应
B.使金属表面光亮,便于观察现象
C.使金属表面温度升高,提高反应温度
(2)有同学提出探究金属活动性强弱还可以依据“金属与金属化合物溶液是否发生置换反应”来判断.为了验证甲、乙、丙三种金属的活动性依次减弱,某同学设计了如下方案:①把甲放入乙的化合物溶液中②把乙放入丙的化合物溶液中③把甲放入丙的化合物溶液中.你认为该方案中的③(填序号)没有必要做.
15.化学用语是学习和研究化学的工具,下列化学用语描述正确的是( )
| A. | 3S表示3个硫元素或3个硫原子 | |
| B. | 氦气的化学式是He | |
| C. | $\underset{N}{•}$H4$\underset{N}{•}$O3中前后氮元素的化合价相同 | |
| D. | 6Fe2+表示6个铁离子 |
12.下列变化属于化学变化的是( )
| A. | 衣服晾干 | B. | 冰雪融化 | C. | 玻璃破碎 | D. | 纸张燃烧 |
19.下列四个图象不能正确反映对应变化关系的是( )
| A. | 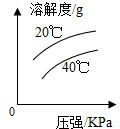 表示氧气的溶解度 | |
| B. | 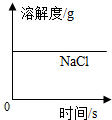 表示恒温蒸发一定量的氯化钠溶液 | |
| C. | 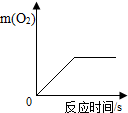 表示加热一定量的高锰酸钾 | |
| D. | 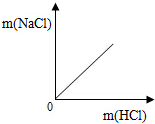 表示向一定量氢氧化钠溶液中滴加稀盐酸 |
9.日常生活中的下列变化中,有一个变化与其他变化的本质不同,该变化是( )
| A. | 浓盐酸挥发 | B. | 活性炭作虑毒剂 | ||
| C. | 蒸汽锅炉受热过度爆炸 | D. | 节日燃放烟花 |
16.下列化学反应发生后,将使用过的仪器浸泡于稀盐酸中,然后用水冲洗,不能将仪器处理干净的是( )
| A. | 盛放石灰水的试剂瓶 | |
| B. | 用一氧化碳还原氧化铁后的硬质玻璃管 | |
| C. | 一氧化碳还原氧化铜后,附有红色固体残渣的试管 | |
| D. | 盛放过生锈铁钉后留下红棕色固体的烧杯 |
13.除去下列物质中的少量杂质,所选用试剂及操作方法均正确的是( )
| 选项 | 物质(括号内为杂质) | 选用试剂 | 操作方法 |
| A | NaCl溶液(Na2SO4溶液) | 适量BaCl2溶液 | 过滤 |
| B | FeCl2溶液(CuCl2溶液) | 足量铁粉 | 过滤 |
| C | CO2(CO) | 过量O2 | 点燃 |
| D | MnO2(KCl) | 足量蒸馏水 | 过滤、蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
 甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答: