题目内容
20.在蜡烛火焰上方罩一只干燥的烧杯,烧杯内壁有水雾出现,证明了( )| A. | 蜡烛中含有水 | |
| B. | 蜡烛燃烧时生成了水 | |
| C. | 可能是空气中的水,不足以证明什么 | |
| D. | 可能都正确,但还要有进一步的实验证明 |
分析 根据题意,在火焰上方罩一只干燥的烧杯,烧杯内壁出现水雾,说明生成了水蒸气解答;
解答 解:做“蜡烛燃烧”实验时,在火焰上方罩一只干燥的烧杯,烧杯内壁出现水雾,说明蜡烛燃烧时生成了水蒸气.
故答案为:B;
点评 本题难度不大,掌握蜡烛燃烧的实验现象、常见气体的检验方法等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献.其生产工艺流程示意图如下:
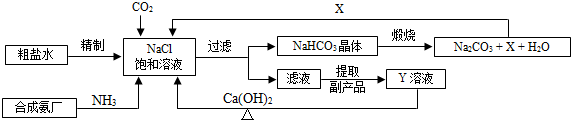
(1)粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制.则加入试剂合理的顺序为NaOH溶液、BaCl2溶液、Na2CO3溶液或BaCl2溶液、NaOH溶液、Na2CO3溶液、盐酸(只写一种).加盐酸的作用是(用化学方程式表示)Na2CO3+2HCl═2NaCl+H2O+CO2↑、HCl+NaOH═NaCl+H2O.
(2)制碱原理为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,该反应原理可看作是由①CO2+NH3+H2O═NH4HCO3和②NaCl+NH4HCO3═NaHCO3↓+NH4Cl两个反应加合而成,则反应类型为复分解反应.
(3)X的化学式为CO2.
(4)Y是滤液中的最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为氯化铵,Y的化学式为NH4Cl,写出Y的一种用途氨气.

(1)粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制.则加入试剂合理的顺序为NaOH溶液、BaCl2溶液、Na2CO3溶液或BaCl2溶液、NaOH溶液、Na2CO3溶液、盐酸(只写一种).加盐酸的作用是(用化学方程式表示)Na2CO3+2HCl═2NaCl+H2O+CO2↑、HCl+NaOH═NaCl+H2O.
| OH- | SO42- | CO32- | |
| Mg2+ | 不 | 溶 | 微 |
| Ca2+ | 微 | 微 | 不 |
| Ba2+ | 溶 | 不 | 不 |
(3)X的化学式为CO2.
(4)Y是滤液中的最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为氯化铵,Y的化学式为NH4Cl,写出Y的一种用途氨气.
11. 晓晓将一盆绿色植株在黑暗中放置了48小时,然后选择其中的一片绿叶进行研究.先剪断叶片的主叶脉(如图所示),再将绿色植株放在阳光下照射2到4小时,发现K处不能正常制造淀粉,其中原因是K处叶片缺少( )
晓晓将一盆绿色植株在黑暗中放置了48小时,然后选择其中的一片绿叶进行研究.先剪断叶片的主叶脉(如图所示),再将绿色植株放在阳光下照射2到4小时,发现K处不能正常制造淀粉,其中原因是K处叶片缺少( )
 晓晓将一盆绿色植株在黑暗中放置了48小时,然后选择其中的一片绿叶进行研究.先剪断叶片的主叶脉(如图所示),再将绿色植株放在阳光下照射2到4小时,发现K处不能正常制造淀粉,其中原因是K处叶片缺少( )
晓晓将一盆绿色植株在黑暗中放置了48小时,然后选择其中的一片绿叶进行研究.先剪断叶片的主叶脉(如图所示),再将绿色植株放在阳光下照射2到4小时,发现K处不能正常制造淀粉,其中原因是K处叶片缺少( )| A. | 叶绿素 | B. | O2 | C. | CO2 | D. | H2O |
8.如图是某市空气固体污染物浓度的等值线图(类似于等高线地形图).据图判断污染最严重的地区是( )


| A. | 甲地 | B. | 乙地 | C. | 丙地 | D. | 丁地 |
15.下列实验中,没有气体产生的是( )
| A. | 向碱式碳酸铜中加入稀盐酸 | B. | 镁带燃烧 | ||
| C. | 将镁带浸在食醋中 | D. | 加热碳酸氢铵 |
5.下列变化中,属于分解反应的是( )
| A. | 铜+氧气$\stackrel{加热}{→}$氧化铜 | B. | 石蜡+氧气$\stackrel{点燃}{→}$水+二氧化碳 | ||
| C. | 过氧化氢$\stackrel{MnO_2}{→}$水+氧气 | D. | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁 |
12.金刚石是( )
| A. | 单质 | B. | 化合物 | C. | 纯净物 | D. | 混合物 |
 如图所示,现有甲、乙、丙、X、Y、Z六种初中化学常见物质,其中连线两端的物质间能发生反应;箭头两端的物质只通过一步反应就能实现转化.已知X、Y、Z都含有同一种元素,且X和Y是组成元素相同的无色液体;甲、乙、丙属于不同类别的物质,其中甲是胃酸的成分,乙的悬浊液常用来涂刷树木以防虫害.则:
如图所示,现有甲、乙、丙、X、Y、Z六种初中化学常见物质,其中连线两端的物质间能发生反应;箭头两端的物质只通过一步反应就能实现转化.已知X、Y、Z都含有同一种元素,且X和Y是组成元素相同的无色液体;甲、乙、丙属于不同类别的物质,其中甲是胃酸的成分,乙的悬浊液常用来涂刷树木以防虫害.则: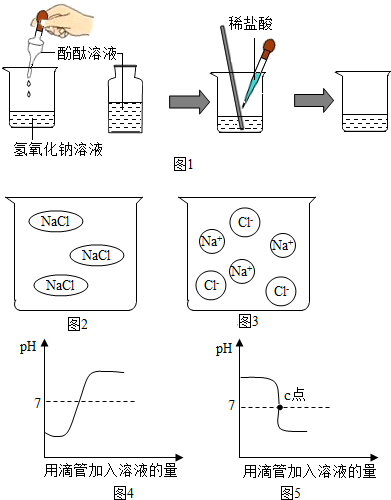 据图填空.
据图填空.