题目内容
19.下列图象与对应的叙述相符合的是( )| A. |  等质量的铁片、铝片分别与足量且质量分数相同的稀硫酸反应 | |
| B. |  向H2SO4和MgSO4的混合溶液中滴加NaOH溶液 | |
| C. |  向pH=13的氢氧化钠溶液中不断加入稀硫酸 | |
| D. |  化学反应中,原子总数随时间的变化 |
分析 A、根据等质量的铁片、铝片分别与足量且质量分数相同的稀硫酸反应金属完全反应等质量的情况下铝生成的氢气比铁要多;铝的金属性比铁强,反应速度快进行分析;
B、根据氢氧化钠与两者都能反应的情况下,在有硫酸的情况下反应生成的沉淀物氢氧化镁不会出现进行分析;
C、根据氢氧化钠和盐酸反应生成氯化钠和水,碱性减弱,pH值减小,反应完全后,显酸性,pH值小于7进行分析;
D、根据质量守恒定律反应前后原子的总数不变进行分析.
解答 解:A、等质量的铁片、铝片分别与足量且质量分数相同的稀硫酸反应金属完全反应等质量的情况下铝生成的氢气比铁要多;铝的金属性比铁强,反应速度快;而图象中铁反应速度快,故A错误;
B、与两者都能反应的情况下因反应生成的沉淀物氢氧化镁溶解于酸,故开始时应无沉淀物生成,故B错误;
C、氢氧化钠和盐酸反应生成氯化钠和水,碱性减弱,pH值减小,反应完全后,显酸性,pH值小于7,故C正确;
D、根据质量守恒定律反应前后原子的总数不变,应是水平线,故D正确.
故选:CD.
点评 本题涉及知识面广,与图象结合理解题意,增加思维空间,题的难度较大,因而能考查学生的知识面掌握程度.

练习册系列答案
相关题目
9.下列物质中有一种与其他三种物质都能发生反应,它是( )
| A. | 锌粒 | B. | 碳酸钙 | C. | 稀盐酸 | D. | 氢氧化钾 |
7.某化学兴趣小组的同学做了如图所示两个实验.下列有关说法正确的是( )
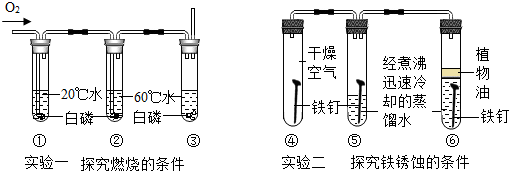

| A. | ①、②号试管中的白磷都不能燃烧 | |
| B. | 久置后,④、⑥号试管中的铁钉都不生锈 | |
| C. | ②、③号试管控制的变量是氧气 | |
| D. | ⑤、⑥号试管中铁钉都没有与氧气接触 |
14. 2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素(部分信息如图所示),填补了元素周期表最后一个空格.下列说法错误的是( )
2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素(部分信息如图所示),填补了元素周期表最后一个空格.下列说法错误的是( )
 2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素(部分信息如图所示),填补了元素周期表最后一个空格.下列说法错误的是( )
2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素(部分信息如图所示),填补了元素周期表最后一个空格.下列说法错误的是( )| A. | 该元素原子的核外电子数为117 | B. | 该元素的原子序数为117 | ||
| C. | 该元素的相对原子质量为294g | D. | 钙和锫都属于金属元素 |
8.说法正确的是( )
| A. | 锌粒与盐酸反应比铁片与盐酸反应要剧烈,故锌比铁活泼 | |
| B. | 酸中一定含有氢元素,所以含氢元素的物质一定是酸 | |
| C. | 燃烧一般都伴随发光和放热现象,所以有发光和放热现象的变化都是燃烧 | |
| D. | 置换反应生成单质和化合物,但有单质和化合物生成的反应不一定是置换反应 |
 某化学兴趣小组在学习了候氏联合制碱法后,运用下图实验装置和其他实验设备成功制得了纯碱--碳酸钠.
某化学兴趣小组在学习了候氏联合制碱法后,运用下图实验装置和其他实验设备成功制得了纯碱--碳酸钠.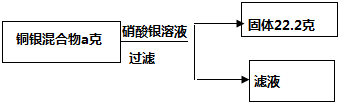 向铜银混合物中,加入溶质质量分数为10%的硝酸银溶液340g,恰好完全反应,请结合图提供的数据计算.求:
向铜银混合物中,加入溶质质量分数为10%的硝酸银溶液340g,恰好完全反应,请结合图提供的数据计算.求: 某同学用稀硫酸、氢氧化钠溶液、酚酞溶液三种试剂,按如图所示进行酸碱中和反应的实验.
某同学用稀硫酸、氢氧化钠溶液、酚酞溶液三种试剂,按如图所示进行酸碱中和反应的实验.