题目内容
10.下列为配制100g质量分数为10.6%的碳酸钠溶液的实验,请分析有关问题:(1)计算:碳酸钠的质量为10.6g.(2)称量:用托盘天平称量.
(3)溶解:用量筒来量取所需的水(水的密度为1g/cm3),量筒的规格是100ml(从下列中选用:10mL、25mL、50mL、100mL).
(4)反思:若称取的碳酸钠中含有水分,则所配制的溶液的质量分数会偏小(填“偏大”、“偏小”或“无影响”).
分析 (1)根据公式:溶质质量=溶液质量×溶质质量分数求解;
(2)根据“左物右码”原则,用托盘天平称量去选;
(3)实验中应根据所取溶液的体积,尽量选用能一次量取的最小规格的量筒.分次量取也能引起误差.如量取89.4mL水应选用 100mL量筒;玻璃棒的作用是搅拌促溶;
(4)根据公式:溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%,若溶质质量减小则溶质质量分数减小.
解答 解:(1)根据公式:溶质质量=溶液质量×溶质质量分数,碳酸钠的质量为:100g×10.6%=10.6g;故答案为:10.6;
(2)根据“左物右码”原则,用托盘天平称量;
(3)实验中应根据所取溶液的体积,尽量选用能一次量取的最小规格的量筒.分次量取也能引起误差.如量取89.4mL水(根据溶剂质量=溶液质量-溶质质量,即:100g-10.6g=89.4g;根据公式:V=$\frac{m}{ρ}$;知该实验需水的体积为89.4mL),应选用 100mL量筒;
(4)因为溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%,所以若称取的碳酸钠中含有水分,即溶质质量减小,则溶质质量分数减小.
答案:(1)10.6;(2)托盘天平;(3)100ml;(4)偏小.
点评 本题综合考查了有关溶液配制的问题,要学会天平和量筒的使用.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
20.物质的用途错误的是( )
| A. | 盐酸:制药 | B. | 氢氧化钠:改良土壤 | ||
| C. | 食盐:制烧碱 | D. | 硫酸铵:作化肥 |
5.为除去下列物质中的杂质(括号内是杂质),所选用的除杂试剂和分离方法都正确的是( )
| 序号 | 物质(括号内为杂质) | 除杂试剂 | 分离方法 |
| A | 硫酸铜溶液(硫酸) | 氧化铜 | 过滤 |
| B | NaOH溶液[Ca(OH)2溶液] | 二氧化碳 | 过滤 |
| C | 二氧化碳(一氧化碳) | 氢氧化钠溶液 | 洗气 |
| D | 二氧化锰粉末(碳粉) | 水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
2.在下列化合物中,铁的质量分数最高的是( )
| A. | Fe2O3 | B. | Fe3O4 | C. | FeO | D. | FeS |
19.如图所示,下列四个坐标示意图分别表示四个实验过程中的某些变化情况,其中正确的是( )
| A. |  加热一定量高锰酸钾的实验,试管中固体的质量变化 | |
| B. | 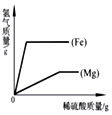 等质量的镁条和铁丝分别与足量的稀硫酸反应,产生气体的质量变化 | |
| C. |  向一定质量的水中加入氢氧化钠时,形成的溶液pH的变化 | |
| D. | 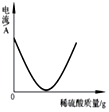 向盛有一定量Ba(OH)2溶液的烧杯中逐滴滴加稀硫酸,测得烧杯中溶液导电性的变化 |
20.由A、B两种元素组成的化合物中,已知A与B的相对原子质量之比为12:1,质量之比为6:1,则该化合物的化学式可能为( )
| A. | AB2 | B. | A2B3 | C. | A2B5 | D. | A2B6 |