题目内容
16.某研究性学习小组利用如图装置探究温度对CO还原Fe2O3的影响(固定装置略).查阅资料:CO2+Zn$\frac{\underline{\;\;△\;\;}}{\;}$CO+ZnO;FeCl3溶液遇KSCN溶液变红.

请回答下列问题:
(1)仪器a的名称是酒精灯,装置B的作用是除去多余的二氧化碳,尾气处理的方法是点燃或收集.
(2)将研究小组分为两组,按如图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D进行加热,其产物均为黑色粉末(纯净物).两组分别用产物进行以下实验:
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入盐酸 | 溶解,无气泡,溶液呈浅黄绿色(含两种金属离子) | 溶解,有气泡,溶液呈浅绿色 |
| 2 | 取步骤1所得溶液,滴加KSCN溶液 | 变红 | 无现象 |
(3)从安全考虑,本实验应在装置A和B之间添加装置E防止倒吸.(填字母编号)
(4)该对比实验结果表明CO的还原能力随温度的升高而增强(填“增强”或“减弱”).
分析 (1)根据常见的仪器名称回答;根据后面要通过F检验CO与Fe2O3反应的产物CO2,分析装置B的作用;根据一氧化碳常见的处理方法分析;
(2)根据信息分析反应物和生成物写出反应的方程式;
(3)根据装置骤冷会引起液体倒流分析;
(4)根据实验的结果分析结论.
解答 解:(1)a是酒精灯;因为后面要通过F检验CO与Fe2O3反应的产物CO2,所以装置B的作用是除去CO中的CO2;尾气中含有有毒气体CO,采用点燃的方法或收集的方法可除去CO;故答案为:酒精灯;除去多余的二氧化碳;点燃或收集;
(2)一氧化碳和氧化铁反应的固体产物为黑色,可能是铁粉、四氧化三铁或二者的混合物;取黑色粉末加入盐酸,甲组观察到黑色固体溶解,无气泡,说明没有铁粉的产生,溶液呈浅黄绿色(含两种金属离子),取步骤1所得溶液,滴加KSCN溶液,变成红色,说明含有氯化铁,另外还产生浅绿色的氯化亚铁,结合反应前后元素的种类不变,还会产生水,因此反应的方程式为:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O;分析乙组现象,乙与盐酸反应产生气体,溶液为浅绿色,因此为铁粉;
故答案为:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O;铁粉;
(3)若A处停止加热后,会使玻璃管骤冷,液体沿着导管倒流进A装置,因此需要在A和B之间加一个倒吸装置;故答案为:A、B;
(4)通过对比甲组和乙组实验可知,乙组使用酒精喷灯使氧化铁还原更彻底,因此该对比实验结果表明CO的还原能力随温度的升高而增强;故答案为:增强.
点评 本题属于信息题的考查,难度较大,特别是方程式的书写,学生不知道思考的方向,因此要细心方向实验的现象进行大胆的猜测并结合相关的知识进行分析是解题的关键.

练习册系列答案
相关题目
18.对于下列几种化学符号,有关说法正确的是( )
①H ②Fe2+ ③Cu ④P2O5 ⑤Fe3+⑥NaCl.
①H ②Fe2+ ③Cu ④P2O5 ⑤Fe3+⑥NaCl.
| A. | 能表示一个分子的是①④⑥ | |
| B. | 表示物质组成的化学式是③④⑥ | |
| C. | ②⑤的质子数相同,化学性质也相同 | |
| D. | ④中的数字“5”表示五氧化二磷中有5个氧原子 |
7.下列关于物质性质及用途的描述中,错误的是( )
| A. | 碳具有还原性,可冶炼金属 | |
| B. | 氧气具有氧化性,可作为燃料 | |
| C. | 氮气的化学性质稳定,可作为保护气 | |
| D. | 石灰石受热分解,可用于制备生石灰 |
4.实验室部分装置如图所示,请回答下列问题.

(1)选择发生和收集O2的装置,填写在下表中(填字母).
(2)如果用MnO2与浓H2SO4加热制备O2,可选用的发生装置是C(填字母).
(3)选用F装置收集气体时,下列实验操作正确的是①②③(填序号).
①反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中
②开始反应后,等到气泡连续且均匀时,再将导管口移入集气瓶
③收集气体后,将集气瓶盖上玻璃片再移出水槽
(4)实验室用KMnO4制备O2的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.若需制备3.2g O2,至少需要消耗31.6g KMnO4.(已知KMnO4的相对分子质量为158)

(1)选择发生和收集O2的装置,填写在下表中(填字母).
| 选用药品 | 发生装置 | 收集装置 |
| H2O2溶液、MnO2 | B | D或F |
| KMnO4 | A |
(3)选用F装置收集气体时,下列实验操作正确的是①②③(填序号).
①反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中
②开始反应后,等到气泡连续且均匀时,再将导管口移入集气瓶
③收集气体后,将集气瓶盖上玻璃片再移出水槽
(4)实验室用KMnO4制备O2的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.若需制备3.2g O2,至少需要消耗31.6g KMnO4.(已知KMnO4的相对分子质量为158)
11.如图是某反应的微观示意图,下列有关说法不正确的是( )
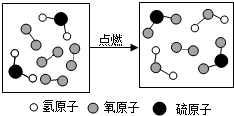

| A. | 生成的物质都是氧化物 | |
| B. | 反应前后原子的种类不变 | |
| C. | 该反应的基本类型属于置换反应 | |
| D. | 反应前后有两种元素的化合价发生了变化 |
1.物质世界充满了变化.下列变化属于物理变化的是( )
| A. | 光合作用 | B. | 煤气中毒 | C. | 冰山融化 | D. | 酸雨侵蚀 |
8.如图为某化学反应的微观示意图,图中“●”表示硫原子,“○”表示氧原子.下列说法中错误的是( )


| A. | 甲是SO2 | |
| B. | 该反应属于化合反应 | |
| C. | 反应前后,分子、原子种类均不变 | |
| D. | 反应中,甲、乙、丙三种物质的分子个数比为2:1:2 |
5.“绿色化学”有助于解决环境污染问题,下列做法不符合“绿色化学”理念的是( )
| A. | 因地制宜,大力发展风力发电 | B. | 废旧电池集中回收,并填埋处理 | ||
| C. | 大力发展公共交通,提倡绿色出行 | D. | 使用可降解塑料,减少“白色污染” |
6.观察是学习化学的重要方法之一,以下是从某同学记录的化学实验现象,其中符合事实的是( )
| A. | 敞开浓盐酸试剂瓶口冒出白雾 | |
| B. | 用pH试纸测得某溶液的pH=1.4 | |
| C. | 铵态氮肥与碱共热放出无色无味气体 | |
| D. | 马铃薯片遇到碘酒后颜色不变 |