题目内容
20.下列实验设计与对应的实验目的表述不一致的是( )| A. | 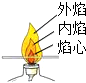 比较火焰各层温度 | B. | 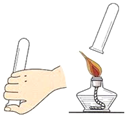 检验氢气的纯度 | ||
| C. | 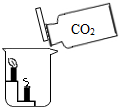 验证CO2的密度比空气大 | D. | 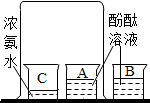 探究空气的组成成分 |
分析 A、根据比较火焰的温度:观察火柴的不同部位被火烧焦的程度分析;
B、根据检验氢气的纯度分析;
C、根据二氧化碳能像倒水一样倾倒得出结论;
D、根据氨气具有挥发性,水溶液能够使酚酞试液变红分析探究的目的.
解答 解:A、通过比较火柴的不同部位的灼烧的程度,可知酒精灯的外焰的温度最高,故表述正确;
B、收集氢气在试管中,用拇指堵住试管口,管口向下移近酒精灯火焰,松开拇指点火,如果听到尖锐的爆鸣声,表明氢气不纯,需要再收集,再检验,直到听到轻微的响声,才表明氢气已经纯净,图中操作正确,故表述正确;
C、下层的蜡烛先熄灭,此操作能验证二氧化碳的密度比空气大,故表述正确;
D、观察烧杯内的酚酞试液变成红色,说明氨气分子在不停的运动,可以探究分子的性质,而不是探究空气的成分,故表述错误.
故选D.
点评 此题比较新颖,综合考查同学们对实验设计与实验目的认识,直观简洁,是一道不错的试题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.襄阳护城河某段水域中氮和磷含量过高,造成水葫芦疯长.这里的“氮”“磷”是指( )
| A. | 分子 | B. | 原子 | C. | 离子 | D. | 元素 |
8.在一个密闭容器中放入X.Y.Z.Q.四种物质,在一定条件下发生化学反应,一段时间后.测得数据如下表,则关于此反应认识错误的是( )
| 物质 | X | Y | Z | Q |
| 反应前质量(g) | 20 | 2 | 1 | 37 |
| 反应后质量( g) | 未测 | 32 | 1 | 12 |
| A. | 物质Z可能是该反应的催化剂 | B. | 反应后物质X的质量为15g | ||
| C. | 反应中Y.Q的质量比是6:5 | D. | 物质Y一定是催化剂 |
15.下列实验现象和对应的结论描述都正确的是( )
| A. | 在某固体中滴加稀盐酸,有气泡产生--该固体一定是碳酸盐 | |
| B. | 在某溶液中滴入碘水或碘酒,变蓝色--该溶液中一定有淀粉 | |
| C. | 在某溶液中滴加硫酸铜加热,无明显现象--该溶液不含葡萄糖 | |
| D. | 向饱和硫酸铵溶液中加入鸡蛋清,产生白色絮状沉淀--蛋白质变性 |
12.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
(1)【演示实验】将一定量的稀盐酸加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式NaOH+HCl═NaCl+H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:NaCl
猜想二:NaCl、NaOH
猜想三:NaCl、HCl
猜想四:有NaCl、HCl和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四.
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、AgNO3溶液、Na2CO3溶液,进行如下三个方案的探究.
【得出结论】通过探究,全班同学一致确定猜想三是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出
【实验探究】(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
①实验操作中的错误是A(填标号A、B、C ).
②实验方案中也有一个是错误的3(填标号1、2、3)
【拓展与延伸】为了更直观地了解“酸碱中和反应”中溶液酸碱度的变化,老师先在烧杯中加入20g40%的氢氧化钠溶液,再逐滴加盐酸,同时用pH计记录溶液的pH值变化,绘制成一下图象
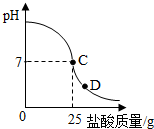 ③所用氢氧化钠溶液中溶质的质量为8g.
③所用氢氧化钠溶液中溶质的质量为8g.
④该盐酸的实际质量分数是多少?(请写出计算过程,结果保留到0.1%)
⑤同学发现装盐酸的试剂瓶上标签注明溶质的质量分数为32%,导致盐酸溶液溶质质量分数改变的原因是:盐酸有挥发性
⑥当滴加盐酸到图象中D点时,烧杯中溶液的溶质是HCl、NaCl(填化学式)
(1)【演示实验】将一定量的稀盐酸加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式NaOH+HCl═NaCl+H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:NaCl
猜想二:NaCl、NaOH
猜想三:NaCl、HCl
猜想四:有NaCl、HCl和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四.
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、AgNO3溶液、Na2CO3溶液,进行如下三个方案的探究.
| 实验方案 | 1、测溶液pH | 2、滴加Na2CO3溶液 | 3、滴加AgNO3溶液 |
| 实验操作 | A | B | C |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 现象:有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有HCl | 溶液中有HCl | 溶液中有HCl |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出
【实验探究】(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
①实验操作中的错误是A(填标号A、B、C ).
②实验方案中也有一个是错误的3(填标号1、2、3)
【拓展与延伸】为了更直观地了解“酸碱中和反应”中溶液酸碱度的变化,老师先在烧杯中加入20g40%的氢氧化钠溶液,再逐滴加盐酸,同时用pH计记录溶液的pH值变化,绘制成一下图象
 ③所用氢氧化钠溶液中溶质的质量为8g.
③所用氢氧化钠溶液中溶质的质量为8g.④该盐酸的实际质量分数是多少?(请写出计算过程,结果保留到0.1%)
⑤同学发现装盐酸的试剂瓶上标签注明溶质的质量分数为32%,导致盐酸溶液溶质质量分数改变的原因是:盐酸有挥发性
⑥当滴加盐酸到图象中D点时,烧杯中溶液的溶质是HCl、NaCl(填化学式)
 结合以下实验室制取气体的常用装置回答下列问题:
结合以下实验室制取气体的常用装置回答下列问题: