题目内容
9.金属是人类生活中常用的材料.(1)下列生活用品中,利用金属导热性的是BC(填字母序号).
A.铝制易拉罐 B.铜制火锅
C.铁锅 D.自行车铁架
(2)为探究锌、铁、铜三种金属的活动性,以及他们和氢元素的位置关系,小明设计了如下实验,你认为可以省略的实验是C(填字母序号).
A.将铁粉放入硫酸锌溶液中; B.将铁粉放入稀硫酸中;
C.将铁粉放入硫酸铜溶液中; D.将铜片放入稀硫酸中.
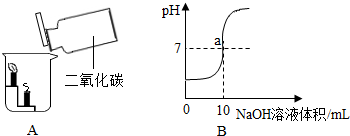
(3)同学查阅资料得知,铜锈主要成分是碱式碳酸铜[Cu2(OH)2CO3,相对分子质量为222],他以铜锈为原料设计并完成如图实验(杂质不与稀硫酸反应,且不含铜元素.图中部分物质略去).

①无色气体A是CO2,溶液C中所含的溶质是FeSO4,固体D的成分是Fe、Cu;
②蓝色溶液B中加入一定量铁粉时,肯定发生反应的化学方程式为Fe+CuSO4═FeSO4+Cu.
分析 (1)根据物质的用途分析性质;
(2)在金属活动性顺序中,氢前的金属能与酸反应产生氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此解答;
(3)根据铜锈的成分结合质量守恒定律分析反应的产物,结合问题回答即可.
解答 解:(1)A.铝可以制易拉罐,说明铝具有良好的延展性; B.铜制火锅是使用了铜的导热性;C.铁锅可以用于炒菜等,说明铁具有良好的导热性;D.自行车铁架,是利用其硬度大;
故填:BC;
(2)通过实验A能证明锌在铁的前面,通过实验B能证明铁在氢的前面,通过实验D能证明铜在氢的后面,从而证明锌>铁>氢>铜,故C可以省略;
故填:C;
(3)①碱式碳酸铜和稀硫酸反应能生成硫酸铜、水和二氧化碳,无色气体是二氧化碳;
向固体D中加入过量稀硫酸时,产生无色气体,是氢气,是由稀硫酸和铁反应生成的,说明铁粉过量,溶液C中所含的溶质是硫酸亚铁;
固体D中含有生成的铜和过量的铁粉;
故答案为:CO2; FeSO4;Fe、Cu;(名称也可)
②蓝色溶液B是硫酸铜溶液,能和铁反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=Cu+FeSO4.
故填:Fe+CuSO4=Cu+FeSO4.
点评 本题考查了常见金属的应用,完成此题,可以依据金属的性质进行,书写方程式时要依据质量守恒定律,难度不大,能够考查学生的综合能力.

练习册系列答案
相关题目
20.下列实验设计与对应的实验目的表述不一致的是( )
| A. | 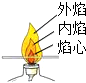 比较火焰各层温度 | B. | 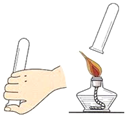 检验氢气的纯度 | ||
| C. | 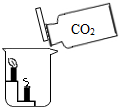 验证CO2的密度比空气大 | D. | 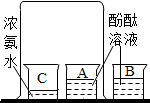 探究空气的组成成分 |
17.下列关于课外生活的一些做法不合理的是( )
| A. | 通过煮沸方法使硬水软化 | |
| B. | NaCl和NaNO2(亚硝酸钠)都有咸味,都可用作食物的调味品 | |
| C. | 在发酵的面团中加入小苏打以提高馒头的口感和除去酸味 | |
| D. | 加热,观察外形变化鉴别热塑性塑料和热固性塑料 |
4.下列各组物质在溶液中能大量共存的是( )
| A. | CaCl2、NH4NO3、Ca(OH)2 | B. | FeCl3、Na2SO4、Mg(NO3)2 | ||
| C. | AlC13、Ba(NO3)2、Na2CO3 | D. | NH4HCO3、AgNO3、BaCl2 |
1.如表列出了除去物质中所含少量杂质的方法,其中正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO2 | CO | 通过足量氢氧化钠溶液,并干燥 |
| B | H2 | 水蒸气 | 通过盛有浓硫酸的洗气瓶 |
| C | N2 | O2 | 通过炽热的木炭 |
| D | NaOH溶液 | Na2CO3 | 加入足量稀盐酸至不再产生气泡 |
| A. | A | B. | B | C. | C | D. | D |
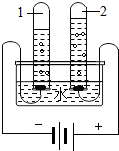 水是宝贵的自然资源,需要珍视.请回答下列问题.
水是宝贵的自然资源,需要珍视.请回答下列问题.